정부가 줄기세포치료제 개발 및 제품화를 위해 적극 지원하기로 했다.
국내에서는 임상 3상 단계의 급성 뇌경색과 척수 손상 치료 등 난치성 질환 관련 5개 품목이 제품화를 앞두고 있어 주목된다.
식품의약품안전처(처장 정승)는 차세대 줄기세포치료제 개발 등을 지원하기 위해 ‘차세대 줄기세포기반제제 평가 연구사업단(2기 연구사업단)’을 운영한다고 27일 발표했다.
연구는 오는 2017년까지 4년간 90억원 예산으로 진행되며, 첫해인 올해에는 임상연구 분석정보 구축 및 차세대 줄기세포치료제의 안전성·유효성 평가를 위한 연구가 예정돼 있다.
2기 사업단은 2017년까지 이들 과제의 확대 연구를 통한 허가 심사 평가법의 표준화 연구 및 임상연구 정보센터 구축 등을 목표로 연구를 진행하기로 했다.
지난 2010년부터 4년간 운영된 1기 연구사업단은 줄기세포치료제의 심사평가지침 및 품질평가 시험법 등을 마련했으며, 세계 최초로 3개의 줄기세포치료제(하티셀그램ㆍ카티스템ㆍ큐피스템) 제품화를 지원했다.
현재 국내에는 이들 3개 줄기세포치료제를 판매하고 있는 파미셀ㆍ메디포스트ㆍ안트론젠 외에 20여 업체가 치료제를 개발 중이다. 그 중 33품목이 임상 진행 중이며, 2상 이상 단계는 10개에 달하고 있다.
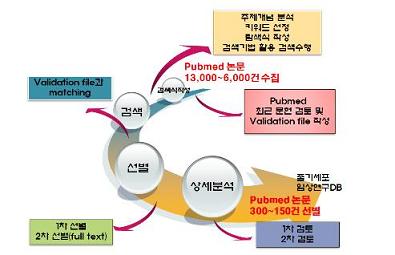
식약처는 "2기 사업단에서는 ▲평가 정보 구축 연구 ▲안전성 평가 연구 ▲유효성 평가 지표 연구 등 15개의 세부과제로 추진된다"며 "국내·외 줄기세포치료제 임상연구 관련 연구논문을 분석, 과학적인 임상시험 설계를 지원하고 개발 동향 분석 기간을 단축할 수 있는 웹 기반의 ‘줄기세포치료제 임상연구 정보시스템’도 구축할 것"이라고 설명했다.
2기 사업단 운영에 따라 식약처는 연구 주제 발표 및 외부 전문가 등이 참여하는 워크숍을 오는 28일 서울 서초구 가톨릭대 의생명산업연구원에서 개최할 예정이다.

