[메디소비자뉴스=오지혜 기자] 올들어 제네릭 개발을 위한 생물학적동등성시험(생동성시험) 승인 건수가 급증한 것으로 나타났다.
식품의약품안전처의 생동성시험 승인 현황에 따르면 올 상반기 70건으로 지난해 동기(47건) 대비 49% 늘어났다.
이는 올 하반기에 재심사(특허)가 만료되는 오리지널 의약품이 많기 때문으로 분석된다. 70건 중 재심사나 특허만료 예정 품목의 생동성시험 승인은 40건(57.1%)으로 조사됐다.
◇승인 57%가 재심사나 특허만료 예정 의약품
개발 성분에선 당뇨병성 다발성 신경염치료제 알티옥트산트로메타민염(제품명 : 덱시드)이 13건으로 1위를 기록했다.
다음으로 당뇨복합제 리나글립틴ㆍ메트폴민염산염(트라젠타듀오) 5건, 항응고제 아픽사반(엘리퀴스) 4건, 항바이러스제 오셀타미비르인산염(타미플루)과 알러지비염치료제 베포타스틴베실산염(타리온) 각 3건 등의 순으로 집계됐다. <표 참조>
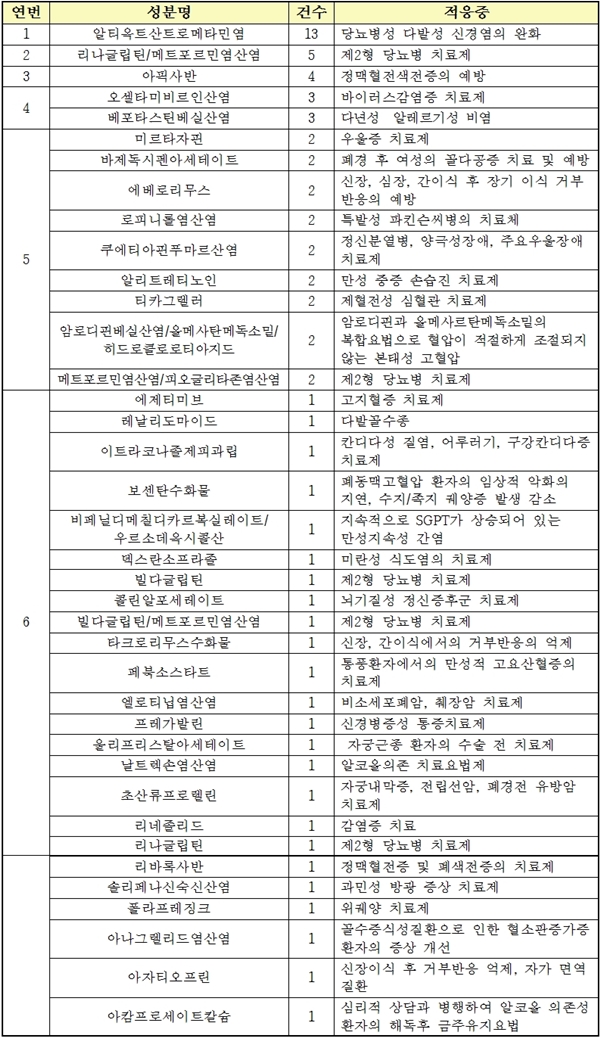
재심사ㆍ특허 만료 예정 품목 중 고령화, 식이 변화 등의 영향으로 당뇨 관련 치료제(23건), 심혈관치료제(6건) 등 만성질환치료제가 높은 비중(29건ㆍ72.5%)을 보였다.
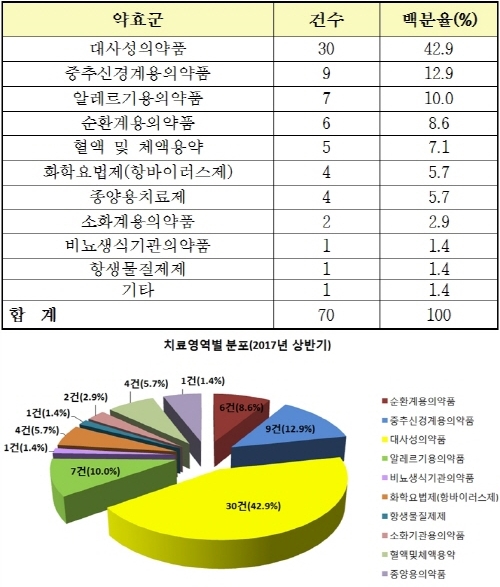
◇대사성약품ㆍ중추신경용제 개발,절반 이상 차지
상반기 치료 영역별 승인 건수는 당뇨치료제 등 대사성의약품(30건ㆍ42.9%), 중추신경계용제(9건ㆍ12.9%)로, 전체의 절반 이상(39건ㆍ55.8%)을 차지했고, 알러지용의약품(7건ㆍ10.0%), 순환계용의약품(6건ㆍ8.6%) 등이 뒤를 이었다.
이 중 중추신경계 의약품은 고령화와 스트레스 등의 영향으로 꾸준히 개발되고 있으며, 항우울제 미르타자핀과 쿠에티아핀푸마르산염, 파킨슨병치료제인 로피니롤염산염이 각각 2건 승인됐다고 식약처는 설명했다. <표ㆍ그림 참조>
식약처 관계자는 "특허만료를 앞둔 의약품을 중심으로 개발이 집중되고 있다"며 "치매 등 노인성 질환과 당뇨, 고혈압, 고지혈증 등 만성질환 치료에 필요한 약 개발 역시 증가세"라고 밝혔다.