의약품안전사용정보시스템 구축ㆍ운영을 지원하기 위한 지침이 개정됐다.
보건복지부와 건강보험심사평가원에 따르면 이달부터 의약품 정보의 확인 및 정보시스템 운영 등에 관한 지침(2016년 12월 제정)이 일부 개정됐다.
의약품 정보는 동일성분 및 금기의약품 여부 등과 연관된 정보를 말한다.
개정안을 보면 동일성분 중복의약품의 DUR 점검은 DUR 성분코드를 기준으로 유효 성분이 동일한 의약품끼리 처방전 간 점검된다.
유효 성분은 내재된 약리 작용에 따라 의약품의 효능 및 효과를 직접 또는 간접적으로 발현한다고 기대되는 물질 또는 물질군으로 주성분을 가리킨다.
안전성 관련 사용중지 의약품은 식품의약품안전처의 안전성 속보 배포 또는 행정처분 등으로 급여 또는 사용중지되는 의약품에 대한 처방전 내 점검이 실시된다.
병용금기 의약품의 경우 식약처 고시에 의거해 함께 사용하면 부작용 발생 등의 우려가 있는 의약품에 대해 처방전 내 및 처방전 간 점검이 실시된다.
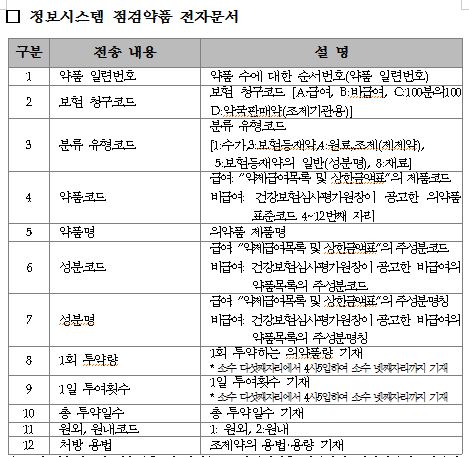
이와 관련해 의사와 약사는 환자에게 처방전을 발행하거나 조제할 때엔 이같은 정보를 심사평가원의 원장에게 전송한다.
심사평가원의 원장은 약사가 전송한 조제 정보를 정보시스템 기준 데이터베이스의 자료와 비교, 그 점검 결과(조제하려는 처방전에 대해 의사가 기재한 처방 사유가 있는 때엔 처방 사유를 포함)를 약사에게 표준팝업창으로 제공한다. <표 참조>
이 지침은 지난 2016년 12월 제정됐다.
오지혜 기자
admin@medisobizanews.com

