희귀의약품이 알짜배기 미래 먹거리로 떠오르고 있다.
희귀의약품은 국내외에서 전체 제약산업에 비해 훨씬 큰 성장률을 보이고 있다. 특히 항암과 바이오의약품 연구가 집중적으로 이뤄지고 있고 대부분 중소벤처기업이 '황금알을 낳는 거위'를 꿈꾸며 개발하지만, 자본과 기술의 한계가 있어 정부의 지원책이 절실한 실정이다.
한국보건산업진흥원은 이같은 산업동향보고서를 12일 발표했다.
보고서에 따르면 국내에서 개발되고 있는 희귀의약품은 대부분 바아오벤처의 초기 임상 단계로 90여개 약물이 있으며 세포치료제 개발 중심으로 활발히 연구하고 있다.
성과도 만만치 않다. 미식품의약국(FDA)의 희귀의약품 지정을 받은 국내 후보물질은 2015년 2건, 2016년 3건, 2017년 9건에서 작년에는 16건으로 크게 증가했다.
희귀의약품은 낮은 유병률로 인해 현재까지는 수익성이 보장되지 않는 특성이 있지만 글로벌시장은 미래를 보고 큰 폭으로 성장하고 있다.<표 참조>

다른 나라들도 개발 단계에서부터 희귀의약품으로 지정, 개발과 개발 후 판매 과정에서 많은 혜택을 부여하고 있다.
미국은 1983년 희귀의약품법 발효 이후 FDA는 개발 단계의 파이프라인들을 심사해 희귀의약품으로 지정하고 있다. 2016년 미국에서 지정된 희귀약은 333개로 10년 전인 2006년 143개 대비 132.8%나 늘었다.
또 연간 접수되는 신청서 대비 지정되는 후보물질의 비율은 10년 간 평균 69.5% 수준으로 높은 편이다. 최근에는 FDA서 희귀의약품 지정 신청을 접수일을 기준으로 업무 일수 90일 안에 무조건 처리하겠다는 목표를 발표, 더 많은 희귀의약품으로 지정될 것으로 예상되고 있다.
이와함께 희귀약 지정 의약품에 대해선 개발 과정에서 개발비 직접 지원, 개발비에 대한 세액 공제, 허가심사 수수료 감면 등 혜택을 주며 개발을 독려하고 있다. FDA는 신약개발을 촉진하기 위해 신속 심사 프로그램을 운영하고 있다.
EU(유럽연합)도 안전성과 유효성에 관한 데이터가 충분하지 않더라도 긴급하게 시판 허가해줘 제한적으로 사용 할 수 있는 '긴급 허가제도'를 운영하고 있다. 일본도 임상연구비 6% 세금 감면(개발사 세금의 10%까지 감면), 임상연구 기금 지원(50%) 등 적극적으로 지원하고 있다.
보고서는 국내 연구가 중소벤처사에 의해 주도되고 거의가 아직 임상 1상 단계인 점을 감안할 때 임상 비용 중심의 연구개발 지원과 세액 공제를 지원해줘야 한다고 주장했다.
2017년 전세계 희귀의약품 시장 규모는 매출액 기준으로 약 1250억달러이며, 2024년까지 연평균 11.3%로 성장해 약 2620억달러의 시장이 형성될 것으로 예측된다. 이는 처방의약품의 글로벌시장 성장률 5.3%의 두 배 이상으로 2024년 전 세계 처방약 매출액의 5분의 1을 차지할 것으로 예상된다.
현재 추세라면 2024년 글로벌 희귀의약품 매출 실적은 세엘진 1위, 존슨&존슨, 노바티스가 각각 2위와 3위를 기록할 것으로 전망된다.
일단 처방 상위 5위 안에만 들면 134억~150억달러 '매출 대박'이 예약돼 있다. 2024년 글로벌 희귀의약품 매출의 약 60% 이상이 상위 10개 업체에서 나올 것으로 보고 있다.
글로벌시장에서 희귀의약품 연구개발을 주도하고 있는 분야는 항암제다. 암치료에 대한 미충족 수요가 높고 질병 발병 기전과 증상이 고도로 세분화돼 있어 환자 수가 적은 틈새 적응증이 많기 때문인 것으로 분석된다.
2016년 미국 제약협회에 따르면 FDA 허가 아래 임상을 진행하고 있거나, FDA의 허가 심사 과정 중에 있는 희귀의약품 566개와 596개 프로젝트가 있다. 이 중 혈액암을 포함한 항암제가 40%를 차지하고 있다.
지난해에는 FDA의 승인을 받은 희귀의약품은 34개 제품으로 이 중 약 38%인 13개의 제품이 항암제이고 10개가 유전질환 치료제, 4개가 감염 관련 치료제다.
국내서도 연구 개발이 활발하다. 식품의약품안전처에 따르면 한국 희귀의약품 생산 규모는 2013년 216억원에서 2017년 595억원으로 급증하고 있다.<표 참조>
녹십자의 헌터라제 생산실적이 압도적으로 많고, 종근당의 펜폴캡슐에 이어 대한약품공업,한미약품,이수앱지스,한국팜비오의 희귀의약품의 생산실적도 10억~20억원대에 달한다.

올 1월까지 희귀의약품으로 지정을 받았거나 지정 대상이 되는 국내 기업 개발 치료제는 93개 성분, 106개의 임상 프로젝트로 확인됐다.
조사된 파이프라인 중 60%(64개)는 바이오의약품이다. 이 중 세포치료제(면역세포 또는 줄기세포)는 31%(20개)로 바이오의약품, 특히 세포치료제가 희귀의약품으로 활발히 연구되고 있다. 치료 영역으론 항암(33.0%), 유전질환(22.6%), 신경질환(10.4%), 자가면역질환(8.5%), 감염질환(7.5%)이 주된 연구개발 적응증이다. 연구개발 단계로는 임상 1상 중인 프로젝트가 30개로 가장 많고, 임상 2상 중인 프로젝트도 26개로 그 다음 순위로 많다.
올 4월까지 한국 제약기업이 개발 중인 약물 중 FDA로부터 희귀약으로 지정을 받은 파이프라인은 36개 성분, 39건이며, 유럽의약품청(EMA)으로부터 지정을 받은 성분은 9개다. <표 참조>
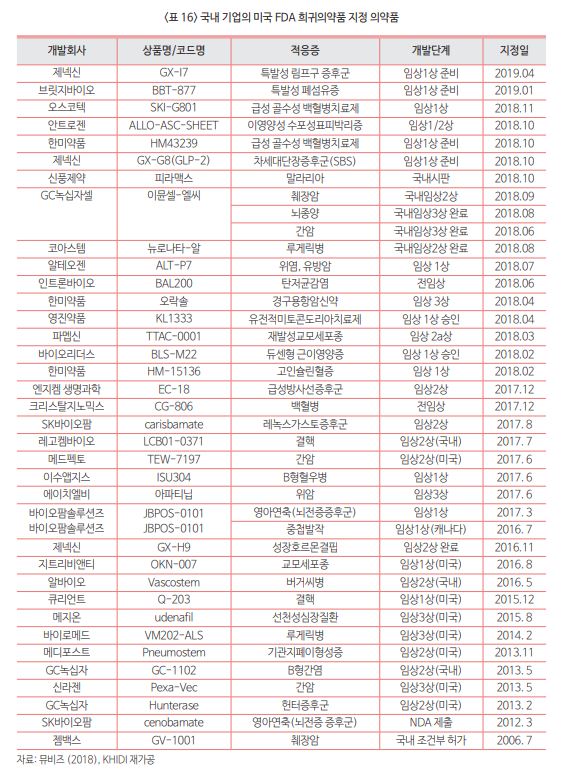
보고서는 "희귀의약품을 개발하는 국내 기업은 대부분 중소 벤처로 기술 이전을 목표로 하고 있다"며 "부광약품, 유한양행, 한미약품처럼 오픈이노베이션을 통해 희귀의약품 분야 사업을 확장하려는 국내제약사들이 글로벌시장의 빅딜을 주도하고 있는 점 등을 감안할 때 정부가 희귀약 성장을 위한 물주기를 확대해야 한다"고 조언했다.

