경구용 장티푸스백신 '비보티프캡슐'(대웅제약) 등 9개 제품이 지난해 국가출하승인 대상 생물의약품으로 허가됐다.
인플루엔자분할백신 '박시플루주사액'(동아에스티) 등 9개 제품은 품목 취하됐다.
식품의약품안전처 식품의약품안전평가원이 최근 발간한 국가출하승인 관련 보고서에 따르면 지난해 세균백신 2개 제품, 바이러스백신 5개 제품, 보툴리눔 톡신 1개 제품, 혈장분획제제 1개 제품이 새로 허가됐다.
신규 허가 제품으로는 비보티프를 비롯해 디프테리아ㆍ파상풍ㆍ백일해ㆍ소아마비 및 헤모필루스 인플루엔자 b형 백신 '인판릭스아이피브이힙주'(GSK), 수두생바이러스백신 '스카이바리셀라주'(SK바이오사이언스) 등이다.
인플루엔자분할백신으로는 '플루플러스테트라프리필드시린지주'(SK바이오사이언스), '비알플루텍테트라주'(보령제약), '테라텍트프리필드시린지주'와 '일양플루프리필드시린지주'(이상 일양약품)가 각각 지난해 허가를 받았다.
백신 외엔 항독소 보툴리눔 '제오민주50단위'(멀츠)와 항파상풍 면역글로불린 '테타불린에스앤프리필드시린지주'(SK플라즈마)도 각각 허가됐다. <표1 참조>

그러나 지난해 세균백신 3개 제품, 바이러스백신 5개 제품, 혈장분획제제 1개 제품은 취하됐다.
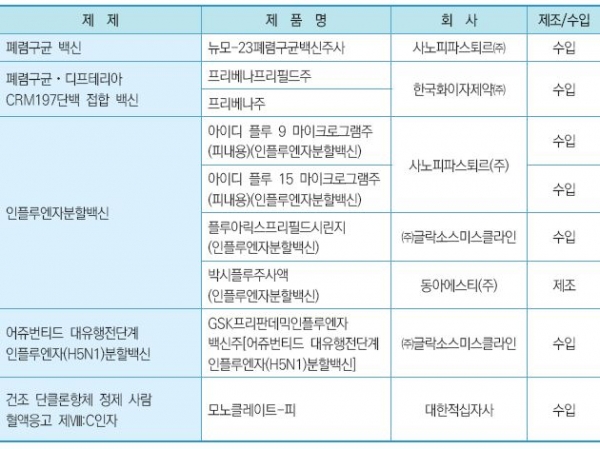
박시플루주사액 외에 '아이디플루9ㆍ15마이크로그램주'(사노피파스퇴르), '플루아릭스프리필드시린지'와 'GSK프리판데믹인플루엔자백신주'(이상 GSK) 등 인플루엔자분할백신과 '프리베나주'와 '프리베나프리필드주'(이상 화이자), '뉴모23폐렴구균백신주'(사노피파스퇴르) 등 폐구균 관련 백신이다.
혈액제제인 '모노클레이트-피'도 취하 제품에 포함됐다. <표2 참조>
국가출하승인 업무는 1953년 중앙방역연구소의 국가검정을 시작으로 국립방역연구소, 국립보건원, 식품의약품안전본부, 식약청을 거쳐 현재 식약처 소속 기관인 식품의약품안전평가원 백신검정과와 혈액제제검정과에서 맡고 있다.
국가출하승인은 백신과 혈장분획제제 등 생물학적제제에 대해 제품을 판매하기 전에 제조단위별로 국가에서 검정시험 및 제조ㆍ품질관리 요약서 등의 자료를 종합적으로 검토해 제품의 품질을 확인하는 제도로, 지난해 말 기준 214개 제품이 대상이다.

