지난해 발암 의심 물질 함유 논란으로 제조 및 판매(급여) 중지 조치된 고혈압약 발사르탄 제제 20개 품목의 급여 중지가 추가 해제됐다. <표 참조>
이에 따라 중지 조치가 해제되지 않고 있는 품목은 22개만 남았다.
보건복지부는 14일 지난해 7월 판매 및 급여 중지된 발사르탄 제제 175품목 중 20품목(10개 제약사)에 대해 급여 재개했다.
앞서 이 제제는 올 5월2일(1차) 106품목에 이어 지난달 4일(2차) 27품목이 조치 해제되면서 조치가 풀리지 않는 품목은 42개만 남았었다.
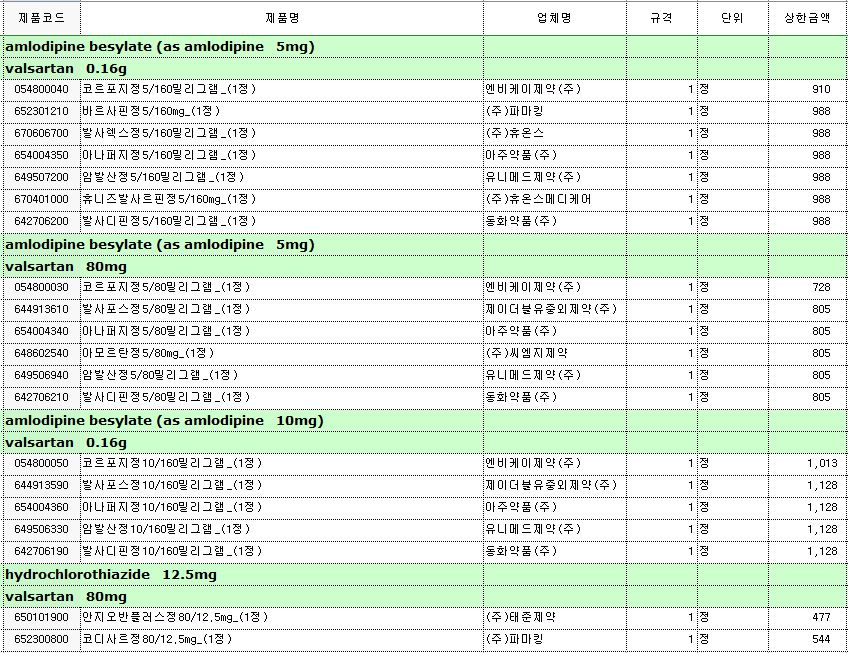
이번에 급여 중지가 해제된 품목은 '코르포지정5/160ㆍ5/80ㆍ10/160밀리그램'(엔비케이제약), '바르사핀정5/160mg'(파마킹), '발사렉스정5/160밀리그램'(휴온스), '휴니즈발사르핀정5/160mg'(휴온스메디케어), '아나퍼지정5/160ㆍ5/80ㆍ10/160밀리그램'(아주약품), '암발산정5/160ㆍ5/80ㆍ10/160밀리그램'(유니메드제약) 등이다.
또 '발사디핀정5/160밀리그램'(동화약품), '발사포스정5/80ㆍ10/160밀리그램'(JW중외제약), '아모르탄정5/80mg'(씨엠지제약), '안지오반플러스정80/12.5mg'(태준제약)도 포함됐다.
복지부는 식품의약품안전처(의약품관리과)가 이들 발사르탄 품목에 대한 판매 중지 등 조치 해제를 알려옴에 따라 해당 제품의 급여도 재개했다.
오지혜 기자
admin@medisobizanews.com

