변비치료제 '레졸로정'(사진ㆍ얀센) 등 '프루칼로프라이드숙신산염' 제제 40개 품목에 대한 허가 사항이 변경된다. <표 참조>

특히 이 제제의 이상반응에 소화불량 등이 신설된다.
식품의약품안전처는 프루칼로프라이드숙신산염(단일제)에 대한 재심사 결과에 따라 허가 사항 변경을 오는 26일까지 의견 조회했다.
국내에서 재심사를 위해 6년간 605명을 대상으로 실시한 시판 후 조사 결과, 이상사례의 발현율은 인과관계와 상관없이 17.7%(605명 중 107명ㆍ144건)로 보고됐다.
이 중 인과관계와 상관 없는 중대한 이상사례는 0.80%(605명 중 5명ㆍ7건)로 조사됐다.
이상반응은 발현 빈도(때때로 0.1~1% 미만)에 따라 소화불량, 당뇨병성 신경병증, 척추공협착, 조절되지 않는 당뇨병, 심실 주기외수축, 가슴 불편감이 보고됐다.
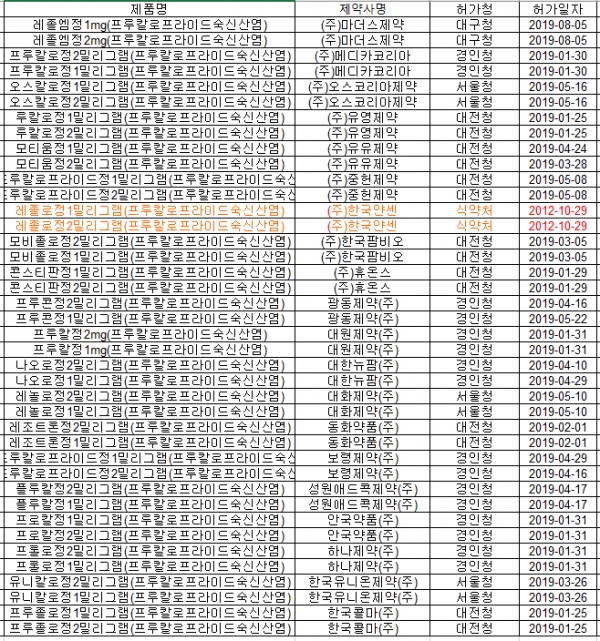
이 제제는 '졸엠정'(마더스제약), '프루칼로정2밀리그램'(메디카코리아), '오스칼로정'(오스코리아제약), '루칼로정'(유영제약), '모티움정'(유유제약), '중헌프루칼로프라이드정'(중헌제약), '비졸로정'(한국팜비오), '콘스티판정'(휴온스), '프루콘정'(광동제약), '프루칼정'(대원제약) 등 40품목이 허가됐다.
또 '나오로정'(대한뉴팜), '레놀로정'(대화제약), '레조트론정'(동화약품), '보령프루칼로프라이드정'(보령제약), '플루칼정'(성원애드콕제약), '프로칼정'(안국약품), '프롤로정'(하나제약), '유니칼로정'(한국유니온제약), '프루졸로정'(한국콜마)도 포함됐다.
김영우 기자
admin@medisobizanews.com

