방사선의약품 '과테크네튬산나트륨' 함유 제제 투여 때 태아 손상 위험으로 임부 투약에 대한 주의가 당부됐다.
식품의약품안전처는 이 함유 제제에 대해 미국식품의약국(FDA)의 안전성 정보 검토 결과에 따라 이같은 허가 사항 변경 지시안을 21일 의견 조회했다.
이와 연관돼 사용상 주의 사항에 '모든 방사선의약품은 태아의 발달 단계 및 방사선량에 따라 태아 손상을 일으킬 수 있어 이 약을 임부에게 사용하려면 임부에게 약물에 따른 방사선량 및 임신 시기에 따라 임신 결과에 이상이 발생할 수 있음을 알려야 한다'고 신설됐다.
식약처에 따르면 이 약이 모유로 이행하는지 여부, 모유 생산 및 수유한 영아에게 미치는 영향에 대한 데이터는 없다.
수유 중인 영아에게 이 약의 노출을 최소화하기 위해 수유부는 투여 후 적어도 3일 동안은 수유하지 않는 게 바람직하고, 수유부는 투약 후 24시간 동안 착유하고 이를 버려야 한다는 것이다.
식약처는 모유 수유의 발달상 및 건강상의 유익성은 이 약에 대한 모체의 임상적 필요 및 이 약 또는 모체의 기저 질환이 수유한 영아에게 끼칠 수 있는 잠재적 위해성과 함께 고려돼야 한다고 당부했다.
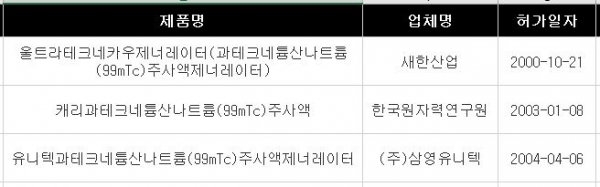
이 제제(용액주사제)는 캐리과테크네튬산나트륨(99mTc) 주사액(한국원자력연구원), 울트라테크네카우제너레이터(과테크네튬산나트륨(99mTc) 주사액제너레이터ㆍ새한산업), 유니텍과테크네튬산나트륨(99mTc) 주사액제너레이터(삼영유니텍)의 3개 품목이 허가됐다. <표 참조>
한편 이 변경안에 대한 의견서는 내달 5일까지 식약처(의약품안전평가과)에 제출하면 된다.