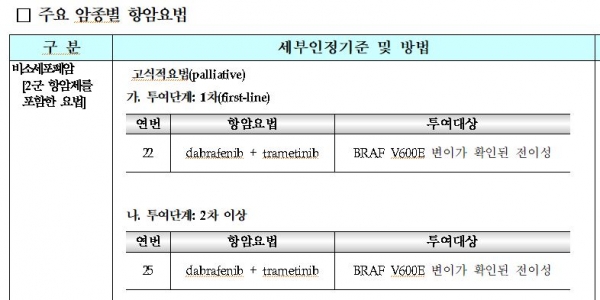
비소세포폐암에 항암제 '다브라페닙ㆍ트라메티닙 병용요법'이 새롭게 건강보험이 적용된다. <표 참조>
건강보험심사평가원은 이같은 '암환자에게 처방ㆍ투여하는 약제에 대한 요양급여 적용 기준 및 방법에 관한 세부 사항' 개정안을 6일 공고했다.
이에 따라 10일부터 비소세포폐암의 이 병용요법과 연관돼 1차와 2차 이상(고식적 요법) 급여된다. 이 병용요법은 흑색종(피부암)에서 폐암까지 건보 확대된다. 비소세포폐암은 폐암의 70% 이상 차지하는 것으로 보고되고 있다.
심사평가원에 따르면 이 병용요법은 2017년 11월부터 유전자돌연변이 'BRAF 600E'가 확인된 전이성 피부암 치료에 급여된 데 이어 2018년 이 변이 비소세포폐암에 적응증이 추가되며 지난해 폐암에 대한 급여 기준 확대가 신청됐다.
급여 확대와 관련해 교과서ㆍ가이드라인ㆍ임상 논문 등을 검토한 결과, 교과서(Cancer 10th)에 신청 요법이 포함된 데다 NCCN(미국종합암네트워크) 가이드라인에서 이 변이가 확인되면 투약 단계 1차 및 2차 이상에 '선호요법(preferred category 2A)'으로, ESMO(유럽종양학회) 가이드라인에서 'IIIA'로 권고돼 이번에 인정된 것이다.
또 이전에 치료받지 않은 BRAF V600E 비소세포폐암 환자를 대상으로 한 2상 연구를 통해 반응률 64%, 무진행 생존 기간 중앙값 10.9개월, 전체 생존 기간 중앙값(mOS) 24.6개월로, 이전 치료에 실패한 BRAF V600E 비소세포폐암 환자를 대상으로 한 2상 연구에서 반응률 63.2%, 무진행 생존 기간 중앙값 9.7개월로 각각 입증됨과 함께 이 변이 비소세포폐암에 투여 가능한 대체약제(표적치료제)가 없어 진료에 필요한 약제로 판단했다고 심사평가원은 설명했다.
이 요법은 의약품 위험분담제도를 통해 급여된 것이다. 위험분담제는 약제 효과나 건보재정 영향에 대한 리스크를 보험자와 제약사가 분담하는 제도다. 이번 급여 기준 확대로 연간 200억원 가량이 추가 소요될 전망이다.