식품의약품안전처(처장 이의경)는 신약 19품목을 포함한 신개발의료기기 등 국내 최초로 허가된 신(新)의료제품의 2020년 1분기 허가 목록을 발표했다.
그동안은 신의료제품 현황을 한눈에 확인할 수 없었으나, 앞으로는 분기별로 발표해 누구나 최근 신의료제품 허가 현황을 간편하게 확인할 수 있다.
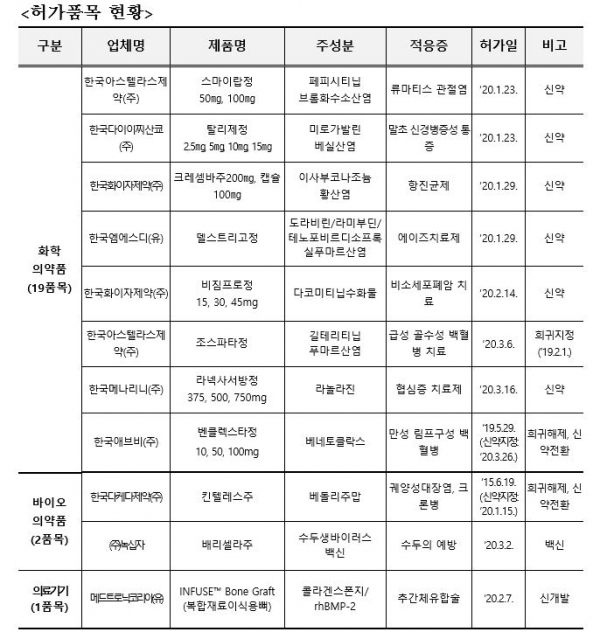
세부 내용을 보면 지난 1분기 동안 신약 19개 품목을 비롯해 국내개발 백신 1개 품목, 신개발 의료기기 1개 품목 등 총 22개 신의료제품이 허가됐다.
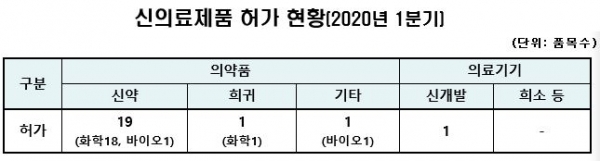
신약의 경우 작년 1분기에 13품목을 허가했던 것에 비해 품목 수가 증가했으며 혈압약이나 항암제 위주에서 류마티스 관절염 치료제, 궤양성 대장염 치료제 등 다양한 효능의 제품이 허가됐다.
주요 신약 허가 품목은 한국아스텔라스제약의 류마티스관절염 치료제 '스마이랍정', 한국다이이찌산쿄의 말초신경병증성 통증치료제 '탈리제정', 한국화이자의 항진균제 '크레셈바주' 등이 있다.<표 참조>
급성 골수성 백혈병에 사용하는 ’조스타파정‘은 희귀의약품으로 허가됐으며 국내에서 개발한 ’배리셀라주‘는 수입에 의존하던 수두 백신의 안정적 공급에 기여할 것으로 보인다. 또한 유전자 재조합 골형성 단백질을 콜라겐 스폰지에 적신 후 추간체에 이식, 새로운 뼈 생성을 유도하는추간체 유합술에 사용하는 의료기기 ’복합재료이식용뼈(INFUSE Bone Graft)‘는 신개발 의료기기로 지정됐다.
식약처는 신의료제품 허가 정보와 관련, "사회적 관심이 높은 품목 등 유용한 정보를 주기적으로 국민에게 투명하게 공개해 국민의 알권리를 강화해 나가겠다"고 강조했다.