식품의약품안전처는 제네릭의약품의 품질 강화와 관리 체계의 효율성을 높이기 위해 현재의 제네릭의약품 허가ㆍ심사 및 사후관리 체계 전반에 대한 개선을 지속 추진한다고 28일 밝혔다.
현재 제네릭의약품들이 위ㆍ수탁 등을 통해 생산 유통되고 있는 상황에서 지금처럼 허가ㆍ심사ㆍ사후관리 체계론 고품질의 제네릭의약품 시장 공급, 의ㆍ약사 및 소비자에게 명확한 정보 제공, 품목 허가ㆍ관리 합리적 효율성을 지속 제고시키기엔 한계가 있는 것으로 지적됐다.
이에 식약처는 '제네릭의약품 국제경쟁력 강화를 위한 민ㆍ관협의체'를 구성, 약 2개월간 운영할 계획이다. 이 협의체는 제약계, 학계, 의사, 약사, 환자, 소비자 단체들로 구성된다. <표 참조>
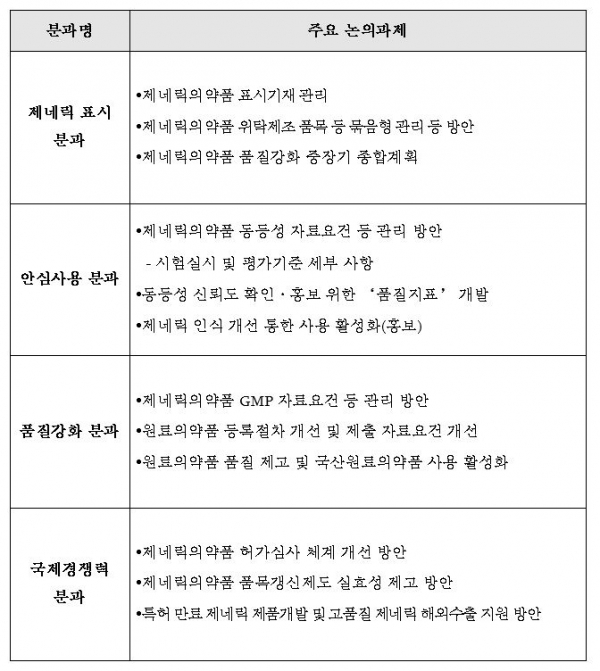
주요 논의 사항은 ▲제네릭의약품 품질 강화 중장기 종합 계획 ▲표시기재 개선 사항 ▲동일 제조소 제네릭의약품 ‘묶음형’ 관리 방안 ▲동등성 자료 요건 등 허가ㆍ심사 규정 개선 ▲GMP 등 품질 개선 ▲제네릭약에 대한 사용자ㆍ소비자 인식 제고 방안 등이다.
식약처는 앞으로도 민ㆍ관협의체 운영 등을 통해 현장의 목소리를 청취, 실효성 있는 제네릭의약품 관리 정책을 마련키로 했다.
오지혜 기자
admin@medisobizanews.com

