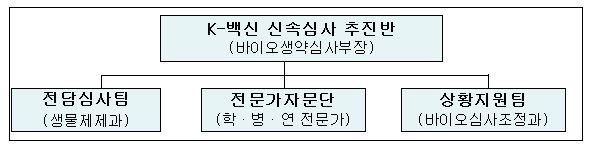
식품의약품안전처는 코로나19 등 감염병 백신 개발 및 허가 단계에서 업계 애로 사항을 최소화하고 시행착오를 줄여 백신이 신속히 출시될 수 있도록 전담 지원하는 ‘K-백신 신속심사 추진반’<그림 참조>을 운영한다고 20일 밝혔다.
식약처에 따르면 백신은 치료제로 사용되는 의약품과 달리 건강한 사람을 대상으로 효과를 확인하게 되기 때문에 신속한 임상 단계 진입을 위해선 허가 기관인 식약처의 전문적인 상담과 방향 제시가 필수적이다.
K-백신 신속심사 추진반은 백신 심사를 총괄하는 ‘전담심사팀’, 내ㆍ외부 업무협력을 주관하는 ‘상황지원팀’, 대한백신학회와 같은 학계ㆍ병원 등의 ‘외부전문가자문단’으로 구성된다.
또 추진반은 기존에 운영 중인 ‘고(Go)ㆍ신속 프로그램’, ‘코로나19 치료제ㆍ백신 개발 범정부 지원단’ 등에서 실무조직으로서도 활동할 계획이다.
식약처는 백신 개발과 환자 치료를 위해 최일선에 있는 산업계, 학계, 병원 등 여러 전문가와 협력, 안전하고 효과 있는 백신이 신속하게 출시될 수 있도록 최대한 지원키로 했다.
오지혜 기자
admin@medisobizanews.com

