식품의약품안전처는 의료기기 유통 구조의 투명성 및 위해 제품 추적성을 강화하기 위해 제조ㆍ수입ㆍ유통 단계별 의료기기 공급 내역 보고를 의무화한 ‘의료기기 공급 내역 보고 제도’를 7월1일부터 본격 시행한다고 24일 밝혔다. <아래 참조>
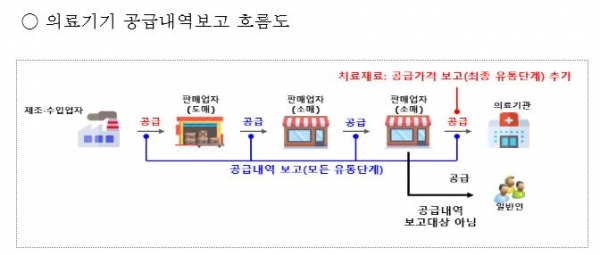
이 제도는 의료기기 제조ㆍ수입ㆍ판매ㆍ임대업자가 의료기기 판매ㆍ임대업자 및 의료기관에 유통할 때엔 공급자 정보, 제품 정보 등을 정보시스템을 통해 보고하는 제도로 인체이식 의료기기와 같이 위험도가 높은 4등급 의료기기부터 단계적으로 시행된다.
만약 공급 내역을 보고하지 않을 때엔 판매업무정지 15일 및 과태료 50만원 등의 처분을 받게 된다.
다만 코로나19로 의료기기 업계의 부담을 덜어주기 위해 올해 12월 31일까지 6개월간 행정처분 대신, 보고 누락업체를 중심으로 제도 안내 및 시정 지시 등을 계도할 예정이다.
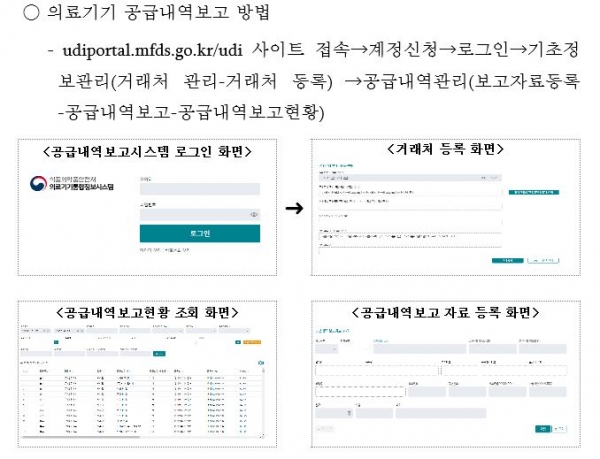
아울러 식약처는 제도 연착륙을 위해 26일 유튜브를 통한 온라인 민원설명회를 개최해 제도 소개, 보고 절차, 의료기기통합정보시스템 사용 방법 등을 안내할 계획이다.
식약처는 앞으로 이 제도 시행에 따라 축적된 공급 내역 빅데이터 등을 활용ㆍ분석해 의료기기 안전관리 체계를 지속적으로 개선해 나가기로 했다.
김영우 기자
admin@medisobizanews.com

