국내 임상시험계획(IND)이 승인된 코로나19 치료제는 글로벌 임상 지원도 가능해 코로나 관련 의약품 개발이 늘어날 것으로 보인다.
코로나19 치료제ㆍ백신 개발 범정부지원위원회(이하 범정부지원위원회)와 업계에 따르면 코로나19 치료제를 개발 중인 제약사 및 바이오업체들이 국내 IND 승인을 잇따라 받은 가운데 일부는 글로벌 임상도 추진하고 있어 정부가 해외 임상 지원도 긍정적으로 검토 중이다.
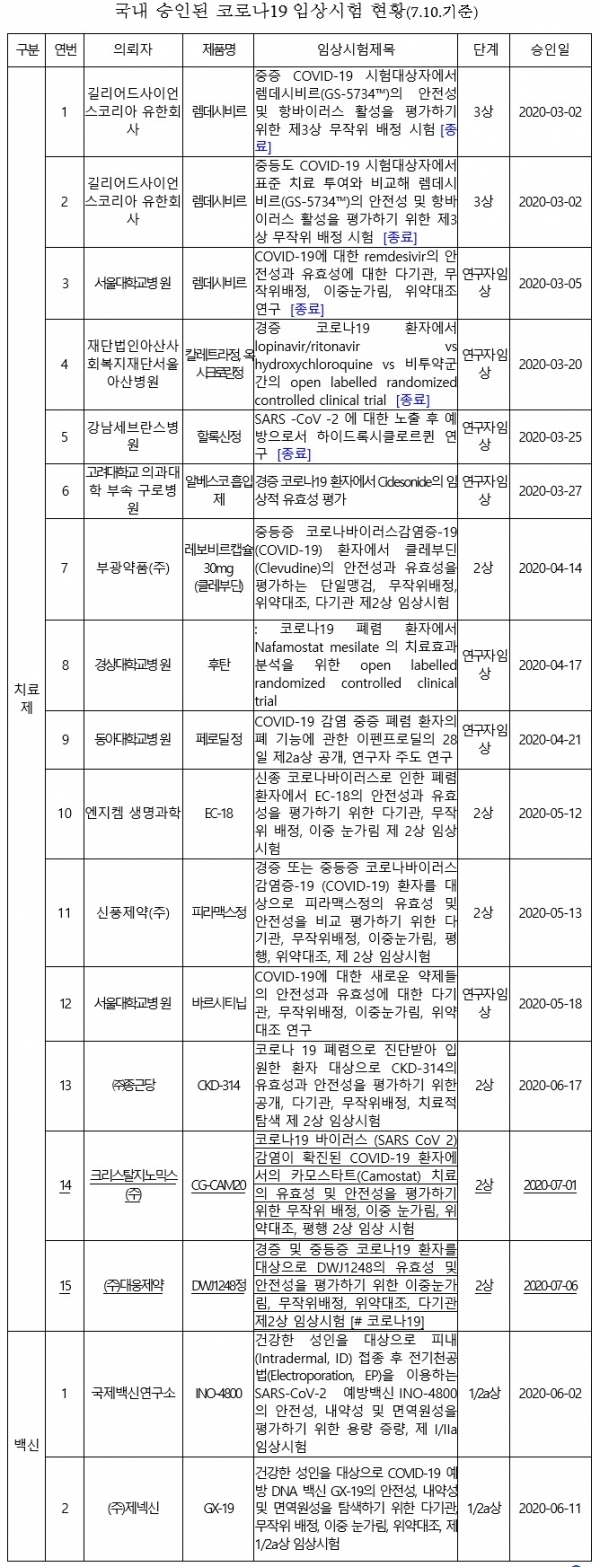
국내에서 승인된 임상은 치료제가 15건(종료 5건), 백신 2건으로 이와 연관된 국내 제약사는 부광약품, 신풍제약, 종근당, 대웅제약 등이며, 약물재창출과 신약 개발을 통해 치료제가 개발되고 있다. <표 참조>
그러나 임상 승인을 받은 치료제 중 글로벌 임상 지원 여부뿐 아니라 환자 연계의 어려움 등이 지적되고 있다.
업계에선 정부가 현재 임상 계획을 심사 중인 코로나19 치료제가 5개이고, 신청을 위해 사전 상담 중인 의약품은 33개로 지원을 강화한다고 했지만, 임상 현장에선 치료제 등 개발에 난관이 적지 않다는 것이다.
이에 따라 국내외 지원을 더욱 늘려야 한다는 게 업계의 주장이다.
이에 대해 범정부지원위원회는 "식품의약품안전처 임상 승인을 받고 글로벌 임상이 추진되고 있는 코로나19 치료제의 해외 개발 관련 지원도 가능할 것"이라고 설명했다.
앞서 제약바이오협회 강당에서 14일 오후 늦게 열린 '범정부 코로나19 치료제 및 백신 개발 지원 대책 설명회'를 통해 보건복지부 임인택 보건산업정책국장도 이같이 밝힌 바 있다.
이날 임 국장은 "이를 위해 국내외 기업 간 협업 개발에 대한 정부 지원도 이뤄질 것”이라며 “지원은 올해로 종료되는 게 아니라 내년에도 올해 못지 않은 지원이 계획돼 있다"고 말했다.
한편 이 설명회에 참가한 기업은 GC녹십자, 보령제약, HK이노엔, 대원제약, 삼진제약, LG화학, 셀트리온, 한국화이자 등 약 30곳에 달했다.