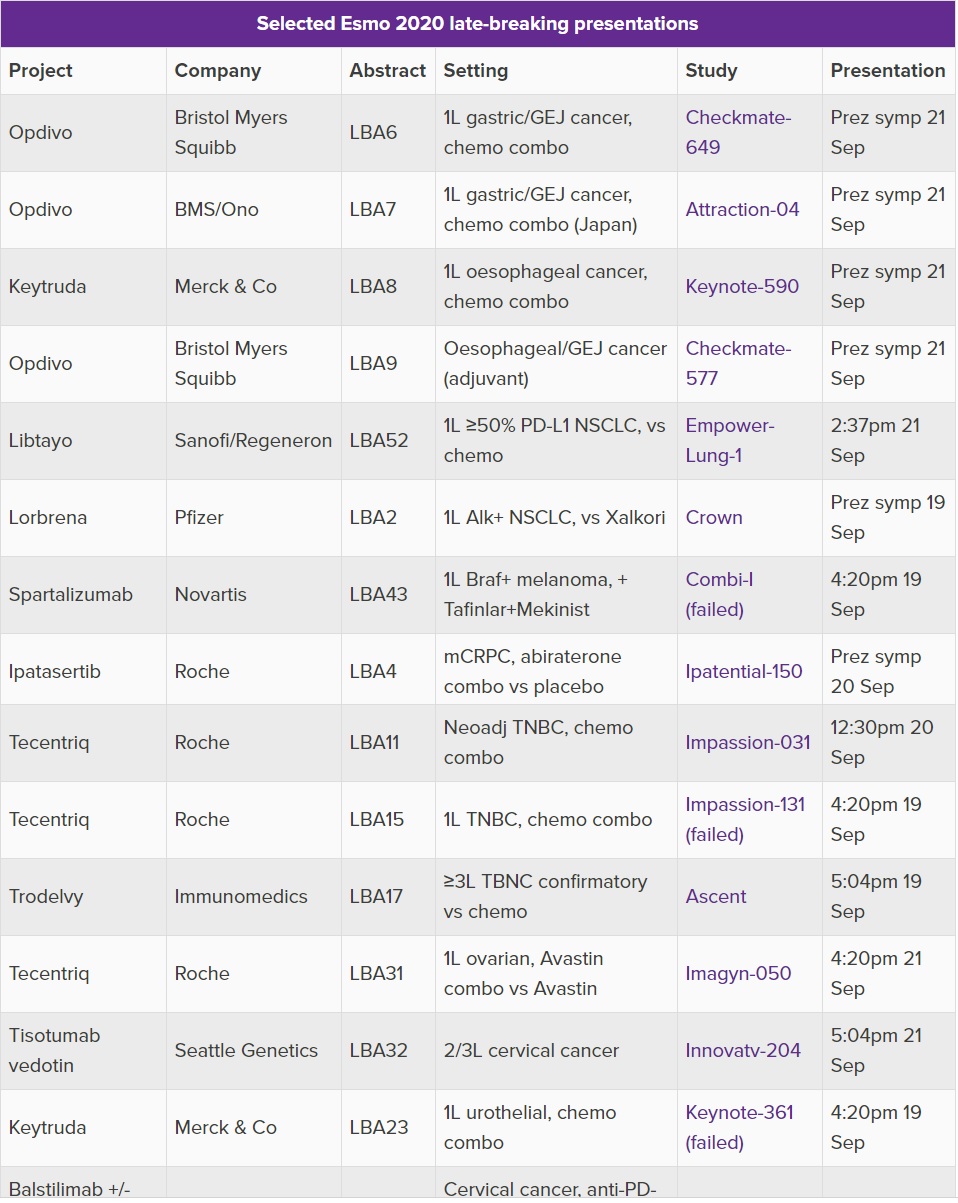
19일 온라인으로 개막하는 유럽종양학회 연례학술회의(ESMO Virtual Congress 2020)에서 MSD의 '키트루다(Keytruda)'와 BMS의 '옵디보(Opdivo)'가 위암에서 치열한 접전을 벌이고 로슈의 '티쎈트릭(Tecentriq)'과 이뮤노메딕스(Immunomedics)의 ‘트로델비(Trodelvy)'가 3중 음성 유방암(TNBC)에서 불꽃 대결을 벌인다.
21일 (현지시간)에 Presidential 세션에서 발표되는 위암 또는 위식도접합암 초록에 키트루다와 옵디보에 관한 4개의 최신임상연구(Late Breaking Abstract)가 올라와 있다.
현재 키트루다는 MAB 중 유일하게 위ㆍ위식도접합암 승인을 받았지만 3차 치료제다. 반면 지난달 BMS 옵디보는 화학요법과 병용요법을 평가한 임상 3상(CheckMate–649)에서 PD-L1 발현 양성(CPS 5 이상) 전이성 위암, 위식도접합부암, 식도 선암에 대한 1차 치료요법으로서 전체 생존기간(OS)과 무진행 생존기간(PFS)에 대한 1차 평가 변수들이 모두 충족시켰다.
그러자 일주일 후 키트루다가 즉각 반격했다. 키트루다는 국소 진행성 전이성 식도암 1차 치료제를 평가한 임상 3상(KEYNOTE-590)에서 1차 최종 목표에 도달, 현재 표준요법인 화학요법과 비교해 전체생존과 무진행 생존에서 통계적으로 개선을 보였다.
이로써 키트루다와 옵디보는 유럽종양학회에서 MSD와 BMS 대표 선수로 흥미진진한 맞대결을 벌이게 됐다.
한편 3중 음성 유방암 치료제 대결도 흥미진진하다.
로슈의 티쎈트릭은 임상 3상(IMpassion 031)에서 화학요법과 병용으로 PD-L1 발현 수준에 관계 없이 병리학적 완전관해율(pCR)을 임상적으로 개선시켰다. 티쎈트릭은 또다른 임상 3상(Impassion-130)에서 아브락산(Abraxane)과 병용요법은 PD-L1 발현 전이성 TNBC 환자를 대상으로 통계적으로 유의한 무진행 생존 혜택을 입증했으며 전체 생존 기간을 임상적으로 의미있는 수준으로 개선시킨 것으로 나타났다. 현재 티쎈트릭+아브락산 병용요법은 PD-L1 발현, 절제 불가능, 국소 진행성 또는 전이성 TNBC 성인 환자의 치료 요법으로 허가돼 있다.
그러나 티쎈트릭과 키트루다는 임상 실패도 함께 맛봤다.
티쎈트릭이 실패한 IMpassion 131 임상이 뒤늦게 부각되고 있는 점이 흥미롭다. 로슈는 티쎈트릭+파클리탁셀과 병용요법이 3중음성유방암 1차 치료요법 임상에서 위약+파클리탁셀보다 무진행 생존기간(PFS) 개선에 대한 통계적 유의성을 입증하지 못했다.
키트루다도 실패의 쓴 맛을 봤다. 키트루다는 진행성 또는 전이성 요로상피암 환자의 1차 요법으로 항암화학요법(시스플라틴 또는 카보플라틴 및 젬시타빈) 병용요법을 평가한 임상 3상( KEYNOTE-361)에서 표준 화학요법 대비 전체 생존기간(OS) 또는 무진행 생존기간(PFS)을 유의한 수준으로 개선시키지 못하면서 1차 평가변수를 충족시키지 못했다.
3중 음성 유방암에서 이뮤노메딕스(Immunomedics)도 만만치 않은 효과를 보였다. 항체-약물 결합체(ADC) ‘트로델비’(Trodelvy)가 3중음성 유방암 임상 3상(ASCENT)에서 강력한 효과를 보여 독립적 데이터안전성모니터링위원회가 만장일치로 연구 중단을 결정해 티쎈트릭의 강력한 대항마로 떠올랐다. 트로델비에 대한 임상 결과는 19일 오후에 발표될 예정이다.
이밖에 시애틀 제네틱스의 자궁경부암 치료제 ‘티소투맙 베독틴’(tisotumab vedotin)은 지난 6월 24%의 치료 관해율(remission rate)을 보여 이번에 승인 신청의 적격 여부와 3차 치료제로 혜택을 따져보는 계기가 될 것으로 예상된다.