근골격계 이완제로 오랫동안 사용돼온 갈라민트주사(사진ㆍ비씨월드제약) 등 '갈라민트리에티오디드(이하 갈라민) 주사제'가 무더기 허가 취소된다.
식품의약품안전처와 보건복지부에 따르면 임상 재평가 자료 미제출(3차)로 이달 21일 갈리치오주(한국유니온제약)에 이어 29일 갈라민트주사 등 7개 품목이 허가 취소(급여 중지)된다.
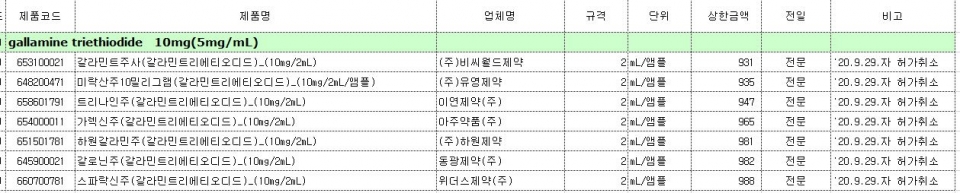
7품목은 갈라민트, 미락산주10mg(유영제약), 트리나인주(이연제약), 가렉신주(아주약품), 하원갈라민주(하원제약), 갈로닌주(동광제약), 스파락신주(위더스제약)로 대부분 20년 만에 시장에서 퇴출된다. <표 참조>
20~30년 전부터 쓰이고 있는 이 품목들은 임상 재평가 대상에 올라 식약처가 재평가 자료를 요구했지만, 해당 제약사들이 끝내 제출하지 않으며 허가 취소(급여 중지)가 결정된 것이다.
이 제약사들은 해당 품목들에 대해 의약품 재평가 자료(임상 결과 보고서)를 제출하지 않아 올초부터 2개월 판매업무정지를 받은 데 이어 2차로도 6개월 판매정지 행정처분을 받았다. 결국 3차도 未제출되며 품목 허가 취소 처분을 받게 됐다.
이 제제 중 매출(작년 기준)은 갈리치오가 약 15억원으로 1위였고, 다음으로 갈라민트가 10억원, 트리나인이 8억원 등의 순으로 집계됐다. 나머지 품목들은 연매출 1억~5억원 안팎을 기록했다.

김영우 기자
admin@medisobizanews.com

