지난해 반짝 높았던 미국 FDA 바이오시밀러 승인이 다시 주저 앉았다.
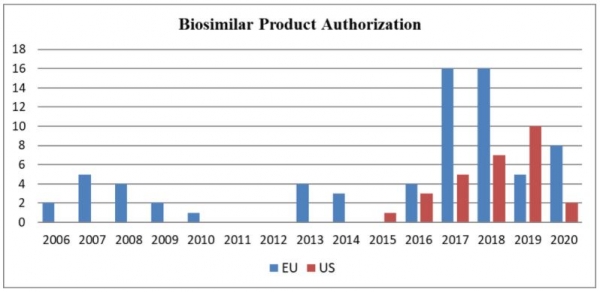
바이오시밀러는 미국보다 유럽이 관대한 시장이었지만, 작년 미국 FDA에서 10개 제품에 대해 승인 스탬프를 찍어 유럽을 역전시켰다. 그러나 코로나19의 영향 등으로 승인이 미뤄지면서 올해는 달랑 2개 제품만 허가를 받았다.
미국 시장에선 올해 4월 이후에는 단 한 개의 제품도 출시되지 않았다. 반면 유럽의약청(EMA)은 ‘노보로그(Novolog)' 첫 바이오시밀러와 3번째와 4번째 ‘아바스틴(Avastin)', 6번째 ‘허셉틴(Herceptin)' 바이오시밀러가 승인을 받아 대조를 보였다.
이처럼 미국에서 바이오시밀러 승인이 어려운 것은 코로나19에 따른 승인 지연도 있지만, 근본적인 제도의 문제점도 해결되지 않고 있기 때문이다.
최근 연구에 따르면 바이오시밀러에 대한 FDA 승인을 얻기 위한 생물학적동등성시험이 오리지널 제품 승인 임상보다 규모도 크고 시험 기간도 길어 비용이 많이 든다. 또 FDA에선 동물 연구를 요구하는 반면 EMA는 생물학적 제품 승인을 위해 동물 연구는 요구하지 않고 있다. 따라서 특허 소송 외에도 이 같은 규제 장벽으로 승인을 늦추고 있는 것이다.
의약품 비용에 대한 언론과 정치적 관심이 증가함에 따라 바이오시밀러 의약품의 중요성은 커지고 있다.
지난해 상위 10개 브랜드 바이오의약품의 글로벌 매출은 약 810억 달러였다. 아이큐비아(IQVIA) 인간 데이터 과학 연구소는 9월 보고서에서 지난 5년(2015~2019년) 동안 140억 달러였던 바이오시밀러 매출이 앞으로 5년 동안 총 800억 달러로 늘어날 것으로 예상했고 바이오시밀러 의약품 사용이 늘면서 미국에서 약제비는 2024년까지 1000억 달러가 절약될 것으로 예측했다.
미국 FDA 약물평가연구센터(CDER) 연례 보고서에 따르면 FDA는 2009년 바이오의약품 가격과 혁신법(BPCIA 일명 바이오시밀러법)에 따라 작년 10개 제품을 승인하면서 바이오시밀러 열기를 부추겼다. 2018년에 발표된 FDA의 바이오시밀러 육성책(Biosimilars Action Plan)은 미국 의약품 지출의 40%를 차지하는 바이오의약품에 대한 경쟁을 높이기 위해 바이오시밀러 시장 개발을 위해 마련된 제도다.
유럽은 2005년부터 바이오시밀러 규제를 유럽의약품청(EMA) 산하 약물사용자문위원회(CHMP)에서 관할한다. 산도스의 ‘소마트로핀(Somatropin)' 바이오시밀러인 성장호르몬 주사제 ‘옴니트로프(Omnitrope)'가 2006년 4월12일에 '바이오시밀러 1호'로 처음 승인된 이후로 69개 품목이 유럽에서 허가됐다. 7개 제품은 승인 후 취소됐다.<아래 그래픽 참조>
미국은 2009년 BPCIA가 제정될 때까지 바이오시밀러 승인이 없었다. 미국 최초의 바이오시밀러 약물이 유럽에서 처음 승인된 지 거의 10년이 지난 후 승인되기도 했다. 산도스의 ‘뉴포젠(Neupogen)' 바이오시밀러인 ‘작시오(Zarxio)'는 2015년에 처음 미국 승인을 받았지만, 유럽에선 이미 9개의 뉴포젠 바이오시밀러인 ‘자지오(Zarzio)'가 2008년에 승인됐었다.
유럽에서는 현재 11개 바이오시밀러 제품이 판매 승인을 위해 EMA에서 심사 중에 있다. 블록버스터 생물 의약품에 대한 특허가 만료됨에 따라 크게 증가하고 있고 미국에서만 26개 이상의 바이오의약품에 대한 바이오시밀러들이 현재 승인을 준비하고 있거나 후기 개발 단계에 있다.
2020년 2월 20일 FDA는 바이오의약품을 모든 단백질을 포함하도록 재정의하면서 크기가 40개 이상의 아미노산 염기서열을 가진 모든 알파 아미노산 중합체로 정했다. 이로 인해 미국에서 바이오시밀러 인슐린 제품이 개방되었다. EMA는 이미 인슐린을 생물학적 제품으로 간주하고 있다. FDA의 이러한 변화는 이미 유럽에서 승인된 많은 바이오시밀러 인슐린 제품이 있고 이 제품을 만드는 기업들이 미국 시장으로 진출할 가능성이 높기 때문이다.
FDA는 보도자료에서 “혁신과 경쟁의 균형을 맞추고 바이오시밀러 및 상호 교환 가능한 제품의 개발 및 승인을 촉진할 계획”이라면서 “안전하고 효과적인 바이오시밀러 및 상호 교환 가능한 제품이 승인을 받으면 경쟁력을 확보하고 환자가 저렴하게 이용할 수 있다”고 발표했다.
FDA는 2020년 6월 11일 ‘란투스’(인슐린 글라진 주사제)의 바이오시밀러 제형인 마일란의 ‘셈글리’(Semglee) 승인했지만 미국 공중보건법(PHS)에 따라 바이오시밀러로 간주되지 않았다. 마일란의 헤더 브레시(Heather Bresch) 최고경영자(CEO)는 “우리는 참조 제품에 이어 FDA 승인을 받고 사노피의 란투스와 동일한 아미노산 염기서열을 가진 인슐린 글라진 치료제를 출시한 최초의 회사가 된 것을 자랑스럽게 생각한다”고 말했다. 그녀는 미국에서 잠재적인 환자 수를 3000만명 이상으로 추정했다.
◇유럽서 승인된 바이오시밀러 제품








◇미국서 승인된 바이오시밀러 제품





