식품의약품안전처(처장 김강립)는 ‘히드로코르티손’ 제제가 조산아를 대상으로 중대한 심장질환을 야기시키는 것으로 나타나 정제와 주사제 등 히드로코르티손 성분제제의 안전성 정보와 관련해 허가사항 변경지시 했다고 8일 발표했다.
이번 식약처 허가사항 변경지시로 2021년 3월 8일부터 허가사항에 소아투여 시 심장계 질환 가능성이 추가된다.
식약처는 “히드로코르티손을 투여한 조산아에서 비대성 심근병증이 나타날 수 있다”면서 “히드로코르티손을 투여한 조산아에서 비대성 심근병증이 보고되었으므로 적절한 진단 평가와 심장 기능 및 구조에 대한 모니터링이 필요하다”고 설명했다.
히드로코르티손은 항염증성 부신피질호르몬제로 전신적인 염증증상을 치료하는 약물로 최근 코로나 중증환자에서 소량의 스테로이드제제가 사망률을 낮추는 것으로 확인되면서 덱사메타손과 함께 효능이 재조명된 바 있다.
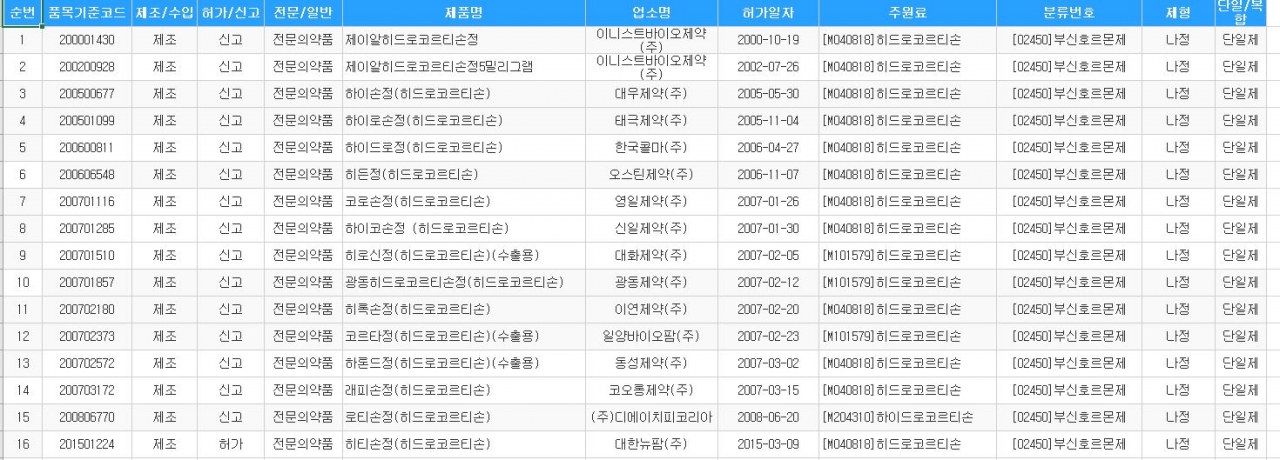
현재 국내에서 허가된 히드로코르티손 정제는 이니스트바이오제약의 '제이알히드로코르티손정' 2종류, 대우제약의 '하이손정', 태극제약의 '하이로손정', 한국콜마의 '하이드로정', 오스틴제약의 '히든정', 신일제약의 '하이코손정', 대화제약의 '히로신정', 광동제약의 '광동히드로코르티손정', 이연제약의 '히록손정', 일양바이오팜의 '코르타정', 동성제약의 '하론드정', 코오롱제약의 '래피손정'과 디에이치피코리아의 '로티손정', 대한뉴팜의 '히티손정' 등 16개 제품이 시판되고 있다.
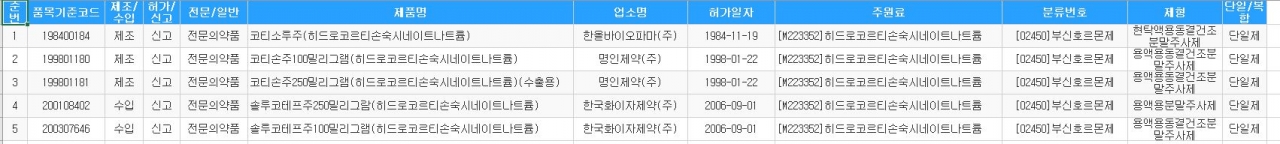
또 주사제는 한올바이오파마의 '코티소루주', 명인제약의 '코틴손주' 100밀리그램과 250밀리그램 2종류, 한국화이자제약의 '솔루코테프주' 100밀리그램과 250밀리그램 2종류 등 총 5개 품목이 판매되고 있다.<표 참조>