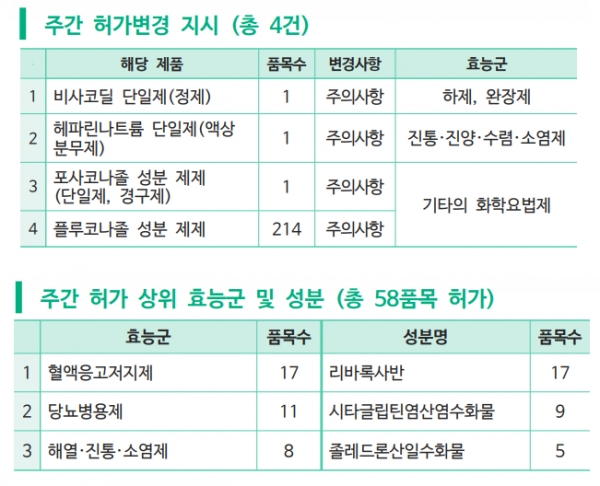
식품의약품안전처는 지난주(3월 22일~28일)에 58개 품목을 신규 허가했다.
약학정보원(원장 최종수)은 30일 발표한 주간 허가리뷰에서 지난주에는 주로 제네릭 제품으로 혈액응고저지제, 당뇨병용제, 해열ㆍ진통ㆍ소염제가 많았다고 밝혔다. 3월 3주 차에 이어 경구용 항응고제인 리바록사반(rivaroxaban) 성분이 17품목(9개 업체)이 허가되었으며 DPP-4 억제제 계열 당뇨병 치료제로 시타글립틴염산염수화물(sitagliptin hydrochloride hydrate) 성분이 9품목(3개 업체)이 승인을 받았다.
또한 비스포스포네이트계 골다공증 치료제인 졸레드론산일수화물(zoledronic acid monohydrate) 성분이 5품목(5개 업체)이 허가되었다. 이 외에도 에토리콕시브(etoricoxib) 성분의 COX-2 억제제 계열 소염진통제인 ‘알콕시아정’(한국엠에스디)의 PMS가 2020년 12월에 만료됨에 따라 ‘알리콕시브정’30mg(알리코제약), ‘엘리콕시브정’30mg(대우제약), ‘에콕시아정’(이연제약), ‘보령에토리콕시브정’30mg(보령제약)이 제네릭으로 허가되었다. 허가된 4개 제품은 알콕시아정이 보유한 결정형 특허를 회피함에 따라 우선판매품목허가권을 부여받게 될 것으로 예상된다.
표재성 혈전 정맥염에 의한 통증 완화에 사용되는 헤파린나트륨 단일제(액상 분무제)의 품목 갱신 자료에 대한 안전성·유효성 검토 결과, ‘2세 미만의 어린이에게는 안전성과 유효성은 확립되지 않았다’라는 내용이 주의사항에 신설되었다. 더불어 이 약을 14일간 투여 후에도 증상 개선이 보이지 않으면 사용을 중단하도록 하는 내용도 추가되었다.
또 항진균제인 플루코나졸 성분 제제의 유럽의약품청(EMA) 안전성 정보 검토 결과, C. albicans 이외 칸디다종 감염의 증가가 보고되어 주의사항에 신설되었다. 이와 관련하여 칸디다종은 플루코나졸에 대한 내재적인 내성이 있거나 감수성이 낮을 수 있으며 이러한 감염은 치료 실패 시 이차적인 대체 항진균 치료가 필요할 수 있다. 따라서 다양한 칸디다종의 내성 발생으로 인한 유병률을 고려해야 한다는 내용이 포함되었다.