식품의약품안전처는 류마티스성관절염 치료제 '토파시티닙' '바리시티닙', '유파다시티닙' 등 3개 성분 제제에 대해 심장마비 등 중증 심질환, 암, 혈전 및 사망 위험이 증가할 수 있다는 '의약품 안전성 서한'을 3일 배포했다.
토파시티닙 등 3개 성분 제제는 면역과 염증을 조절하는 효소인 야누스키나제(Januskinase, JAK)를 억제하는 약물인 JAK억제제로서 관절염 또는 궤양성 대장염 등 만성 염증성 질환 치료제로 사용된다.
이번 안전성 서한은 지난 1일 미국 식품의약국(FDA)이 확인ㆍ검토한 결과 안전성 서한에 관련한 정보를 국내 의약 전문가와 환자에게 제공하기 위해 마련됐다.
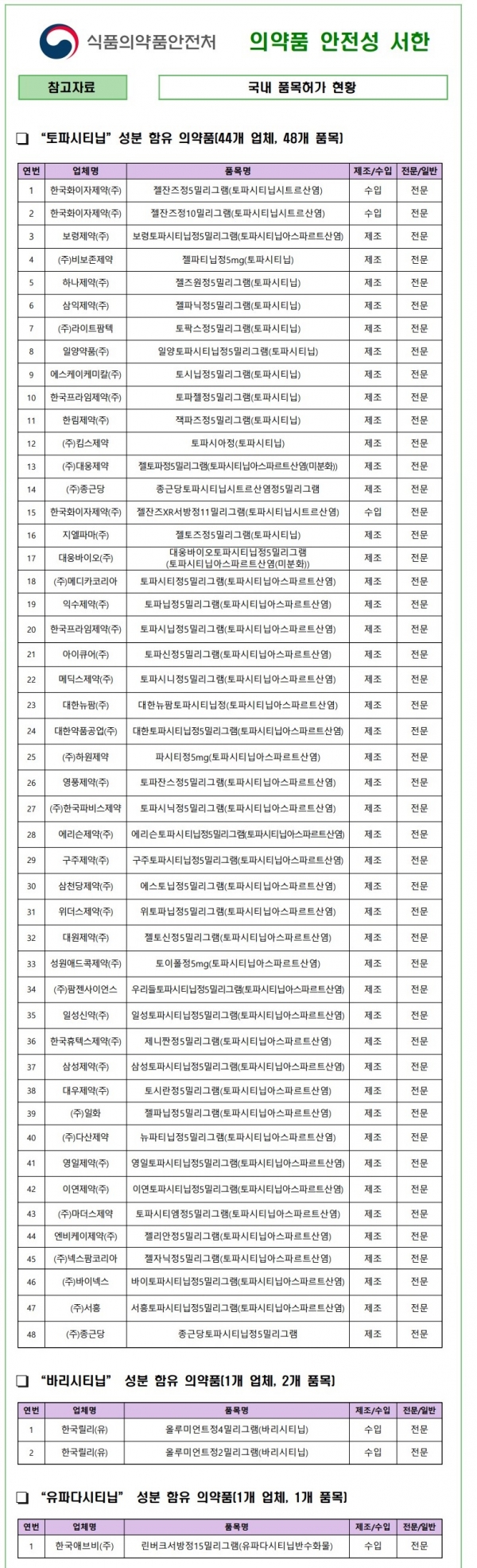
대상품목은 ▲토파시티닙 (한국화이자제약, 비보존제약,하나제약,삼익제약,라이트팜택, 일양약품, SK케미칼, 한국프라임제약, 한림제약, 킴스제약, 대웅제약, 종근당, 지엘파마, 대한약품공업, 메이카코리아, 익수제약, 아이큐어, 메딕스제약, 대한뉴팜, 하원제약, 영풍제약, 한국파비스제약, 에리슨제약, 구주제약, 삼천당제약, 위더스제약, 대원제약, 성원에드콕제약, 팜젠사이언스, 일성신약, 한국휴텍스제약, 삼성제약, 대우제약, 일화, 다산제약, 이연제약, 엔비케이제약, 넥스팜코리아, 바이넥스, 서흥,대웅바이오 등 44개 업체ㆍ48개 품목), ▲바리시티닙 (한국릴리(유) '올루미언트정4밀리그램' 등 1개 업체ㆍ2개 품목), ▲유파다시티닙 (한국애브비 '린버크서방정15밀리그람' 등 1개 업체ㆍ1개품목)이다.<표 참조>
식약처에 따르면 미국 FDA(식품의약국)가 토파시티닙 성분 제제 안전성 관련 대규모 무작위 임상시험을 검토한 결과, 해당 제제 복용 시 심장마비나 뇌졸중, 암, 혈전, 사망 등의 위험이 증가함을 확인한 것으로 나타났다. 또 토파시티닙과 동일한 기전을 가진 바리시티닙, 유파다시티닙 성분 제제도 유사한 위험을 수반할 것으로 간주된 것으로 확인됐다.
이에 식약처는 3개 성분 제제에 대해 박스경고에 중증 심질환, 암, 혈전, 사망의 위험을 추가하고 제제 복용 개시 또는 지속 시 환자의 유익성ㆍ위해성을 고려할 것을 권고했다. 또 TNF 억제제에 반응하지 않거나 내약성이 없는 특정 환자에게만 사용하도록 사용을 제한할 것도 강조했다.
식약처 관계자는 "국내 외 허가현황, 사용실태 및 문헌자료 등을 종합 검토하여 필요한 경우 조치사항을 추가로 안내할 예정"이라며 "국내 병ㆍ의원에서는 해당 제제를 환자에게 투여할 경우 안전 정보를 반드시 확인할 것”을 요청했다.