비알콜성지방간(NASH) 전 세계 환자가 4억4400만명에 이르지만 승인 받은 치료제가 없는 거대한 블루오션 시장이다.
미국 국립보건원은 미국 내 NASH 환자 수를 전체 인구의 12% 수준인 3000만명으로 예상하고 있다. 크레딧 스위스(Credit Suisse) 투자은행은 2030년 전 세계 NASH 시장을 200억 달러(약 23조5060억원)로 전망하고 있다.
NASH는 성인 4명 중 1명이 발병하는 비알코올성 지방간 질환(NAFLD) 중 간세포에 염증이 보이는 만성 진행성 간 질환이다. 질병이 진행되면 간 섬유화 및 간 기능 장애로 이어질 우려가 있고 간 섬유증, 간경변, 간암의 주요 원인의 하나다. 비알코올성지방간질환(NAFLD)은 알코올 섭취와 무관하게 간에 지방이 쌓인 상태로 비코올성단순지방간(NAFL), NASH, 간경변증을 포괄하는 개념이다.
NASH는 자각 증상이 거의 없어 진단이 어렵다. 현재 치료벋은 식이 요법과 운동 요법 등 생활 습관의 개선에 의한 체중 감소와 당뇨병이나 고혈압 같은 합병증의 치료가 전부다. 간 기능 부전에 이른 경우 치료법은 간 이식 밖에 없다. 인도 제약사 자이두스 카딜라(Zydus Cadila)가 당뇨병 치료에 1차적으로 사용되는 ‘사로글리타자’(saroglitazar)를 인도에서 NASH 치료제로 세계에서 첫 승인을 받았지만 미국과 유럽에서 승인된 치료제는 없다.
◇NASH 치료제 국내서 9개 제약사 개발
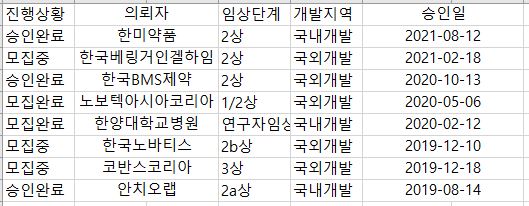
10월 19일 식품의약품안전처 의약품통합정보시스템에 따르면 NASH 치료제 임상 단계에 있는 곳은 한미약품 등 9곳이다. 한미약품이외에 한국베링거인겔하임, 한국비엠에스제약, 노보텍아시아코리아, 한양대학교병원, 코반스코리아서비스유한회사(CRO), 한국노바티스, 세엘진, 안지오랩 등이 포함됐다.
이 중 개발 단계가 가장 빠른 곳은 코반스코리아서비스다. 이 회사는 임상시험수탁기관(CRO)으로 임상 중인 ‘아람콜’(Aramchol)의 국내 유통 및 판권은 삼일제약이 갖고 있다. 삼일제약은 2016년 이스라엘 갈메드(Galmed)와 NASH 치료제 아람콜 국내 유통 및 판매 라이선스 제휴를 맺은 바 있다. 아람콜은 현재 미국, 유럽, 남미, 아시아지역 등에서 2000여명을 대상으로 글로벌 3상 임상(ARMOR study)이 진행 중이며 최근에는 갈메드가 FDA로부터 아람콜 메글루민 3상을 추가로 승인받았다.
한미약품은 현재 간 생검(liver biopsy)으로 질환이 확인된 NASH 환자들을 대상으로 위약 대비 치료 유효성, 안전성, 내약성 등 확인을 위한 임상 2상을 미국 및 한국에서 진행하고 있다. 특히 한미약품은 FDA 독립적 데이터 모니터링 위원회(iDMC)로부터 LAPSTriple Agonist(랩스트리플아고니스트)의 글로벌 임상 2상을 계획 변경 없이 계속 진행하라는 권고를 받아 상용화를 위한 개발에 박차를 가하고 있다. LAPSTriple Agonist는 체내 에너지 대사량을 증가시키는 글루카곤, 인슐린 분비 및 식욕 억제를 돕는 GLP-1, 인슐린 분비 촉진 및 항염증 작용을 하는 GIP 수용체를 동시에 활성화하는 혁신 신약으로 NASH 영역에서 게임체인저의 잠재력을 갖추고 있다는 평가를 받고 있다.
종근당도 국내 판권을 확보한 NASH 치료제인 ‘나모데노손’(Namodenoson)이 글로벌 임상 2b상에 진입했다. 나모데노손의 개발사인 이스라엘 바이오벤체인 캔파이트 바이오파마(Can-Fite Biopharma)가 최근에 투자설명서를 통해 나모데노손이 NASH 적응증과 관련해 임상시험심사위원회(IRB)의 글로벌 임상2b상의 심사를 통과해 올 4분기에 환자등록이 시작될 것으로 발표했다. 나모데노손은 NASH과 간세포암(HCC) 적응증으로 개발되고 있는 신약 물질이다. 종근당은 2016년 캔파이트 바이오파마로부터 간세포암 치료제로서 국내 독점 공급 및 판매권 계약을 체결했으며 2019년 2월 NASH 치료제로 추가 계약을 맺었다.
NASH 치료제를 개발하는 업체 중 바이오벤쳐도 있다. 퓨쳐메디신은 핵심파이프라인이 NASH 치료제 후보물질 'FM101'이다. 올해 4월 헝가리에 이어 9월에는 스페인 규제 당국으로부터 임상 2상 승인을 받았다. 퓨쳐메디신은 정낙신 서울대학교 약학과 교수가 2015년 창업했다. 이 회사는 이달 초에 코스닥 상장예비심사 청구서를 제출했다.
이외에도 안지오랩은 비알코올성 지방간염(NASH) 환자를 대상으로 ALS-L1023의 안전성 및 유효성을 탐색하기 위한 다기관, 무작위배정, 이중 눈가림, 위약 대조 임상 2a상에 있으며 한국베링거인겔하임과 한국비엠에스제약은 임상 2상, 한국노바티스는 임상 2b상을 진행하고 있다.
◇글로벌 제약사들도 개발 포기 잇따라
NASH는 인슐린 저항과 산화 스트레스 등 여러 요인이 관계하고 있어 각 인자에 대한 다양한 표적 치료제가 개발되고 있지만 개발 난이도가 높아 지금까지 많은 후보 물질이 개발 포기를 선언했다.
2019년에는 길리어드의 ASK-1 억제제 ‘셀론서팁’(selonsertib)이 임상 3상에서 실패했다. 임상 3상까지 진행했던 프랑스 젠핏(Genfit)의 PPARα/β 작용제 ‘엘라피브라노’(Elafibranor)도 쓴 맛을 봤다. 또 올해 처음 허가를 받을 것이라 예상됐던 인터셉트의 ‘오칼리바’(Ocaliva 오베티콜릭산)는 FDA로부터 부정적인 의견을 들었다.
애브비의 경구용 CCR 2/5형 길항제인 ‘세니크레바이록’(cenicriviroc)도 개발이 중지되었고 일본의 다나베 미쓰비시 제약도 올해 개발한 선택적 미네랄코르티코이드 수용체 ‘MT-3995’의 개발을 중단시켰다.
미국 인터셉트社의 ‘오칼리바’(Ocaliva 오베티콜산)는 최초의 NASH 치료제가 될 것으로 기대받고 2019년에 미국과 유럽에서 신청했으나 이듬해 6월에 미국 FDA가 “이익이 위험을 상회하지 못한다”면서 승인을 보류했다. 이 약은 중등도~중증 섬유화를 동반한 환자를 대상으로 한 임상에서 간 섬유화를 유의하게 개선 했지만 효과를 얻을 수있는 환자는 제한되어 있고 부작용으로 높은 빈도로 가려움이 확인되었다. 인터셉트는 FDA와 협의를 계속하고 있으며 유망한 추가 데이터가 나오면 다시 신청할 계획이다.
일본 다이닛폰스미토모제약(大日本住友製薬)은이 한국과 일본에서 개발ㆍ판매권을 취득했지만 2018년에 권리를 반환했다.
◇릴리의 ‘터제파타이드’ 등이 선두권
일라이 릴리(Eli Lilly)가 개발하고 있는 GLP-1과 GIP 수용체에 작용하는 이중 작용제 ‘터제파타이드’(tirzepatide)가 2형 당뇨병 대상 시험의 하위 연구에서는 인슐린 제제와 비교하여 간 지방 함량을 개선하는 효과를 입증했다. 비슷한 기전을 가진 약제로는 독일 베링거 인겔하임 및 덴마크 제약기업 질란트 파마(Zealand Pharma)가 NASH 치료제로 개발을 진행 중인 글루카곤 유사 펩타이드-1(GLP-1)/글루카곤 이중 작용제 ‘BI 456906’이 올해 6월 FDA 패스트 트랙 심사대상으로 지정받았다. 현재 BI 456906은 성인 NASH 지방간염 및 당뇨병을 동반하거나 동반하지 않는 간 섬유증 치료제로 임상 2상을 진행 중이다.
가장 빠르게 임상 3상에 들어간 약물은 현재 미국 마드리갈 파마슈티컬스(Madrigal Pharmaceuticals)의 THR-beta 작용제 ‘레즈메티롬’(resmetirom)과 덴마크 노보 노 디스크의 ‘세마글루타이드’ (Semaglutide) 등이 있다. 마드드리갈 파마슈티컬스는 갑상선 호르몬 수용체 (THR) -β 작용제 레즈메티롬가 비침습 진단 및 바이오 마커에 대한 비맹검 임상에서 간 지방과 섬유화, 염증을 감소시키는 효과가 있다고 밝히면서 위약 대조 임상 3상에 기대를 걸고 있다. 이 약은 2022년에 승인 신청할 계획이다.
노보 노디스크의 '세마글루타이드'는 올해 중등도~중증 섬유화를 동반 환자 1200명을 대상으로 글로벌 임상 3상을 시작했다. 이 약은 2형 당뇨병과 비만 치료제로 승인된 GLP-1(글루카곤 유사 펩타이드-1) 수용체 길항제로 임상 3상에서 NASH 치료와 간 섬유화 개선 등 조직학적 개선을 평가하는 파트 1과 간 관련 복합 이벤트 위험 감소를 평가하는 파트 2로 나누어 진행한다. 노보 노디스크는 파트 1 데이터가 나오는 단계에서 이미 끝낸 임상 2상 결과와 함께 신청할 예정이다.
노바티스(Novartis)는 NASH 치료제 임상 2상 후보물질 '트로피페소'(tropifexor)와 SGLT1/2 억제제 '리코글리플로진'(licogliflozin) 병용요법으로 임상 2상을 진행 중이다.
이밖에 미국 BMS가 ‘페그벨퍼민’(Pegbelfermin)을 개발하고 있다. 페그벨퍼민은 인간 섬유 성장인자(FGF21)의 페길화 아날로그(peglated analogue) 피하주사제로 제2형 당뇨병을 동반한 비만 환자의 대사질환 및 간 섬유화증 개선을 위한 핵심 마커로 평가받고 있다. 이미 전임상에서 NASH에 대해 간내 지방증, 염증, 간세포 팽창, 섬유화 개선 효과를 보인바 있다.

