지난주(11월 15일~21일)에 식품의약품안전처로부터 승인을 받은 약물 중 가장 눈에 띄는 것은 한국화이자제약의 백혈병 치료제로 ‘마일로탁주4.5mg’이다.
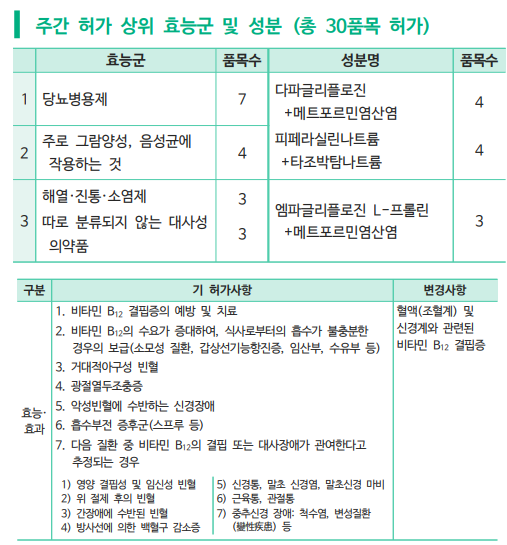
약학정보원(원장 최종수)은 지난주에는 당뇨병용제 7개 품목 등 총 30개 품목이 식약처 승인을 받았다고 발표했다.
주간 허가 리뷰에 따르면 마일로탁주는 겜투주맙 오조가마이신(gemtuzumab ozogamicin) 제제로 CD33 항원을 표적으로 하는 항체-약물 접합체(ADC)다. CD33을 발현하는 종양세포와 결합하여 세포독성 약물인 N-아세틸-감마-칼리키아마이신 디메틸하이드라지드(N-acetyl-γ-calicheamicin dimethylhydrazide)를 세포 내로 방출시켜 DNA 절단을 통해 종양세포의 사멸을 유도한다. 마일로탁주4.5mg은 새로이 진단된 CD33-양성의 급성 골수성 백혈병(AML) 성인 환자의 치료에 사용하도록 승인되었다.
급성 골수성 백혈병 성인 및 소아 환자의 약 85~90%가 CD33 양성으로 알려졌으며 이 환자군에서 유용한 타겟요법으로 기대되고 있다.
한편 주간 허가변경 명령은 2건으로 '코바마미드' 단일제(주사제)의 품목 갱신 자료를 검토한 결과 효능ㆍ효과에 대한 허가사항 변경 명령이 있었다. 기존 효능ㆍ효과인 ‘비타민 B12 결핍증의 예방 및 치료’ 등 7가지에 해당하는 적응증에서 ‘혈액(조혈계) 및 신경계와 관련된 비타민 B12 결핍증’에 사용하도록 효능ㆍ효과가 변경되었다.
오지혜 기자
admin@medisobizanews.com

