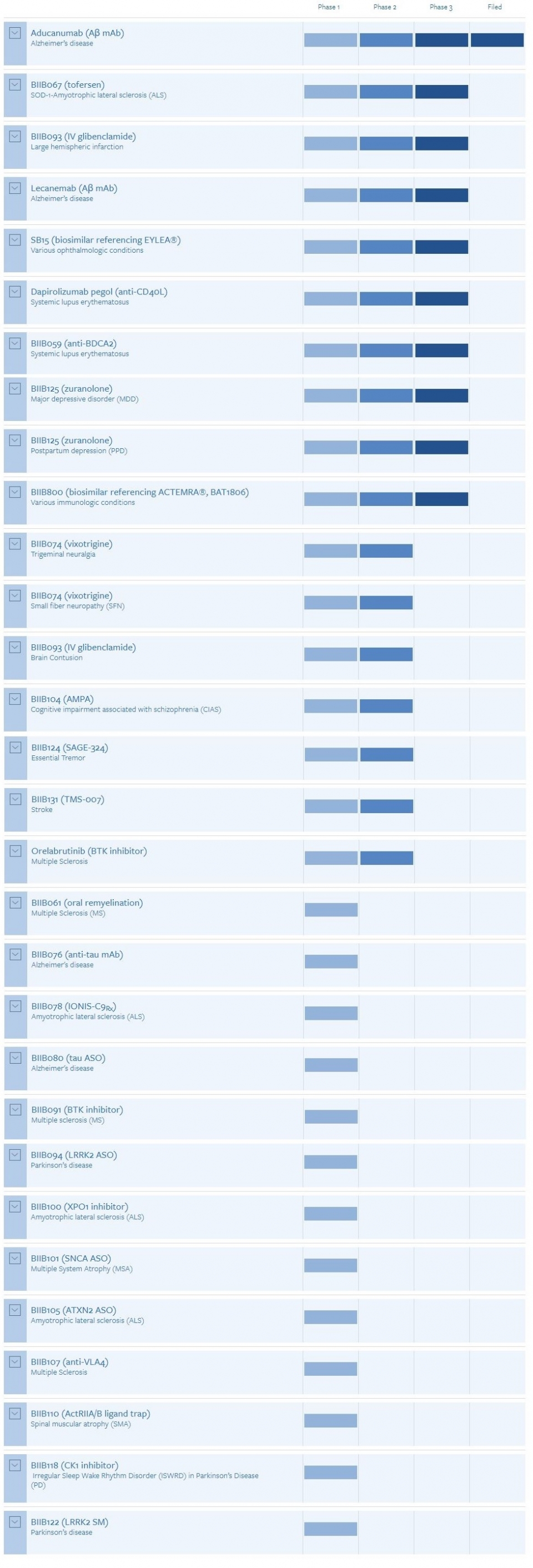
삼성바이오로직스가 30일 공시를 통해 "미국 바이오기업 바이오젠 인수와 관련된 보도는 사실이 아니다"라고 부인을 했지만 삼성이 알츠하이머 치료제 ‘에듀헬름’(Aduhelm 아두카누맙ㆍ사진)으로 유명한 미국 바이오젠 인수한다는 보도가 외신을 통해 알려지면서 바이오젠의 파이프라인에 관심이 높아지고 있다. 바이오젠은 현재 에듀헬름을 포함 30개 파이프라인을 두고 개발하고 있다.<아래 그래픽 참조>
그 중에서도 가장 관심이 큰 것은 역시 알츠하이머 치료제 파이프라인이다. 바이오젠과 에듀헬름을 공동개발하고 있는 일본 에자이는 최근 에듀헬름 유효성 논란 속에 숨겨놓은 핵심 파이프라인은 ‘레카네맙’(lecanemab)에 두고 있다는 보도가 나왔다.
닛케이(日経)비즈니스는 27일 미국 제약사 바이오젠 일본법인이 제출해 후생노동성에서 심의 중인 에듀헬름 승인이 불확실 하자 ‘후속타’로 레카네맙에 희망을 걸고 있다고 밝혔다.
12월 22일에 개최된 후생노동성 약사ㆍ식품위생심의회 의약품제1부회는 에듀헬름에 대해 “유효성 여부를 판단하기 곤란하다”면서 추가 데이터를 요구하고 있다. 하지만 에듀헬름 임상시험 데이터를 제출하기 위해서는 새로운 임상을 해야하기 때문에 몇 년 뒤에나 가능하다.
후생노동성에서 심의 내용을 발표한 22일 에자이 주가는 전일 종가 7122엔에서 9% 하락하여 6477엔이 됐다. 하지만 에자이 주가가 다시 기지개를 켜고 있다. 24~27일에 걸쳐 상승해 27일 종가는 6666엔이 되었다.
이 같은 주가 상승 배경에는 바이오젠과 공동 개발하고 있는 또 다른 알츠하이머병 신약 물질 레카네맙이 24일 미국 FDA로부터 패스트트랙(fast-track)으로 지정되어 우선 심사를 받게 됐기 때문이다. 레카네맙은 항 아밀로이드 베타(Aβ) 원시섬유(protofibril) 항체로 에듀헬름과 비슷한 기전이다. 업계에선 이전부터 유해성이 적은 레카네맙이 더 유력하다는 여론이 많았다.
에듀헬름은 아밀로이드 베타라는 단백질을 제거하는 항체 의약품이다. 알츠하이머병 환자는 뇌 속에 아밀로이드β가 축적되는 것으로 알려져 치매 전 단계나 발병 초기에 이것을 제거하여 환자를 치료한다. 다만 아밀로이드β가 뇌 속에 쌓이는 것이 알츠하이머병 원인이라고 하는 것은 아직은 가설에 지나지 않는다.
바이오젠과 에이자이는 알츠하이머병 중증화 억제를 입증하기 위해 가벼운 인지 장애나 치매 초기 환자에게 에듀헬름을 투여하는 임상을 해왔다. 그런데 2개의 임상에서 상반된 결과가 나왔다. 첫 번째 임상에서 중증화를 억제시켰지만 다른 임상에서는 유효성을 입증하지 못했다. 그럼에도 불구하고 미국 FDA는 2021년 6월, 뇌 속 아밀로이드β 축적이 감소했다는 데이터를 근거로 조건부 신속 승인을 했다.
이번 후생노동성 전문부회에서는 아밀로이드β 축적과 질병 증상과의 관계가 명확하지 않은 것도 논란이 되었다고 한다. 에듀헬름은 올해 12월 유럽에서도 승인이 거부되었다. 바이오젠은 유럽에서 재심사를 청구하고 일본에서도 규제 당국과 추가 데이터에 관한 협의를 할 생각이지만 에듀헬름에 대한 부정적 의견이 많아 큰 기대를 걸 수가 없는 실정이다.
바이오젠에 따르면 7~9월 애두헬름 매출은 30만 달러에 그쳤다. 이 같은 판매 부진으로 바이오젠은 미국에서 에두헬름 가격을 내년 1월부터 약 50% 낮춘 2만8200 달러로 내린다고 발표했다. 바이오젠 주가도 미국에서 에듀헬름 승인 직후의 고가 대비 40% 이상 하락하고 있다.
이러한 배경으로 바이오젠과 에자이는 에듀헬름의 후속 버전인 레카네맙에 기대를 걸고 있다. 레카네맙은 뇌 속에 축적된 아밀로이드β를 제거하도록 제작된 항체 의약품으로 에듀헬름과 마찬가지로 아밀로이드β가 알츠하이머병의 원인이라는 가설에 기초하여 개발됐다. 1000명이 넘는 알츠하이머병 환자를 대상으로 한 대규모 임상시험은 아직 진행 중이지만 미국에서는 신속 승인 취득을 향해 9월부터 FDA 신청데이터 제출을 시작했다.
레카네맙은 피험자 800명을 대상으로 한 임상시험에서는 일부 효과가 인정되었다. 무엇보다 에듀헬름에서 높은 빈도로 발생한 뇌의 붓기나 출혈 등의 부작용이 적었다. 에듀헬름 부작용은 후생노동성 전문부회 심의에서도 논란이 된 것 외에도 미국에서 판매가 부진한 요인이기도 했다.
의료 현장에서도 레카네맙 승인을 기대하는 목소리가 높다. 2022년 9월에 1800명에 가까운 환자를 대상으로 대규모 임상 3상을 이어가면서 FDA에서 신속심사 신청을 내년 전반기에 마칠 예정이다. 치매의 60~70%를 차지하는 알츠하이머병을 치료하는 획기적 신약이 나올지 관심이 쏠리고 있다.