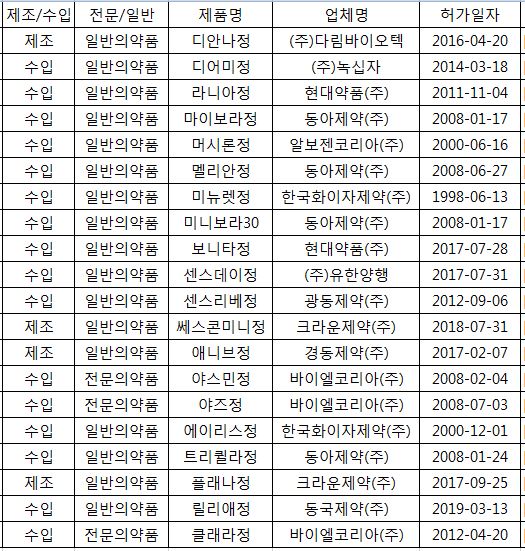
식품의약안전처는 미국식품의약품국(FDA)의 '복합경구피임제' 관련 안전성 정보에 대한 검토 결과 허가 변경이 필요하다고 판단하고 변경안을 마련했다고 21일 공지했다. <주요 피임약 표 참조>
식약처는 ‘데소게스트렐‧에티닐에스트라디올’ 복합제의 경우 35세 이상 흡연자와 선천성 또는 후천성 과응고병증 환자엔 투약하지 말도록 했다.
또 35세 이상의 여성은 복합경구피임제 투여 시작 전에 심혈관계 질환 또는 정맥혈전색전증의 위험을 증가시킬 수 있는 고혈압ㆍ당뇨ㆍ이상지질혈증ㆍ비만을 고려해야 한다고 주의를 줬다.
‘게스토덴‧에티닐에스트라디올’ 복합제는 선천성 또는 후천성 과응고병증 환자와 35세 이상 흡연자는 투약하면 안된다고 밝혔다.
‘레보노르게스트렐ㆍ티닐에스트라디올’ 복합제의 경우에는 혈전 등 심혈관계 부작용의 위험성을 증대시키며 이 위험성은 나이와 흡연량(1일 15개비 이상)에 따라 증가되고 특히 35세 이상의 여성에게 현저하게 나타난다며 투약 금지 경고를 했다. 선천성 또는 후천성 과응고병증 환자도 금지했다.
이밖에 ‘드로스피레논ㆍ에티닐에스트라디올’ 복합제도 흡연은 혈전증 등 부작용을 증대시킨다고 주의를 주며 선천성 또는 후천성 과응고병증 환자도 금지할 것을 권고했다.
식약처는 내달 5일까지 검토 의견을 제약사와 관련 협회 등에 통지하고 허가 변경을 할 것으로 알려졌다.
박찬영 기자
asch123@hanmail.net

