대표적 과민성 방광치료제로 꼽히는 베타미가서방정(사진ㆍ아스텔라스제약)이 '요저류' 등 이상사례 185건이 보고됐다.
요저류는 오줌이 모두 배출되지 않은 채 남아있는 증상을 뜻한다.
식품의약품안전처에 따르면 베타미가서방정25ㆍ50mg의 재심사 결과를 바탕으로 미라베그론 제제에 대한 허가 사항 변경 지시안이 이같이 마련됐다.
식약처는 국내에서 재심사를 위해 6년간 3145명을 대상으로 실시한 시판 후 조사 결과, 이상사례(이상반응)의 발현율은 인과관계와 상관없이 5.18%(3145명 중 163명ㆍ총 185건)로 나타났다고 설명했다.
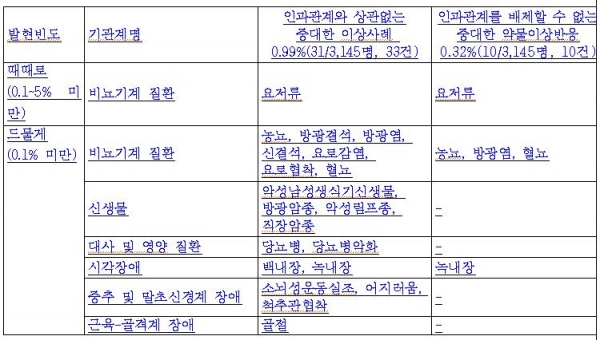
이 중 인과관계와 상관없는 중대한 이상사례 및 인과관계를 배제할 수 없는 중대한 약물이상반응은 발현 빈도에 따라 요저류 포함 비뇨기계 질환(농뇨ㆍ방광결석ㆍ방광염ㆍ신결석ㆍ요로감염ㆍ요로협착ㆍ혈뇨), 신생물(악성남성생식기신생물ㆍ방광암종ㆍ악성림프종ㆍ직장암종), 대사 및 영양 질환(당뇨병ㆍ당뇨 악화), 시각장애(백내장ㆍ녹내장), 중추 및 말초신경계 장애(소뇌성운동실조ㆍ어지러움ㆍ척추관협착), 근육-골격계 장애(골절) 등이 보고됐다. <표 참조>
베타미가서방정은 지난 2014년 국내 출시된 후 연매출 500억원 넘게 기록 중이다.
한편 이 허가 사항은 내년 초 반영될 예정이다.
김영우 기자
admin@medisobizanews.com

