세계 최대 생명공학기업 중 하나인 버텍스(Vertex)가 실험약물 ‘VX-864’의 테스트를 중단했다. 이는 ‘알파-1 항트립신(AAT)’이라는 폐 보호 단백질 결핍 유전질환 치료제다. 버텍스는 지난해 10월에도 간 효소 증가 등을 이유로 ‘VX-814’의 테스트를 중단한다고 발표했었다.
버텍스는 10일(현지시간)“ 실험 대상 환자의 간 및 폐 건강에 필수적인 단백질을 크게 증가시킬 수 있다는 사실을 발견했기 때문에 이 실험은 긍정적”이었다면서 “이 결과가 AAT 결핍 질병 치료 방법에 대한 회사의 기본 이론을 입증한다”고 말했다.
그러나 “환자에게 실질적으로 도움이 될만큼 충분히 강력하지 않다는 문제가 있어 테스트를 중단하기로 했다”고 덧붙였다.
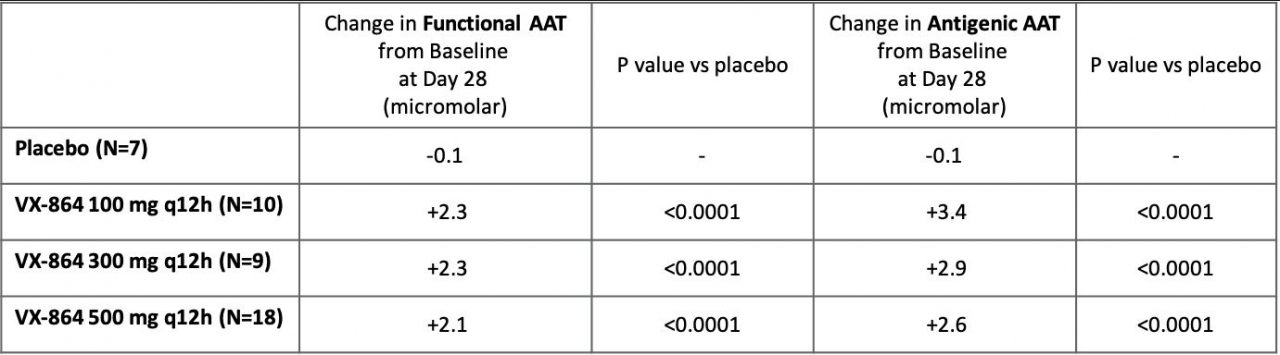
VX-864의 연구에서 테스트된 모든 약물 투여량은 위약과 비교해 단백질의 기능 수준이 ‘ 통계적으로 유의미한 증가’를 나타냈다. 구체적으로, 버텍스 약물로 치료받은 환자는 위약에 비해 기능성 단백질이 평균 2.2~2.3 마이크로몰 증가했다. 그러나 질병을 예방할 수 있다고 추전하는 11마이크로몰 보다는 현저하게 적어 실망을 자아냈다.
그리고 이전 모델인 VX-814와 달리 VX-864는 안전 문제를 유발하지 않았다. 버텍스는 이 약물이 일반적으로 내약성이 뛰어나며 1명을 제외한 모든 환자가 치료를 완료했다고 말했다. 회사는 어떤 환자도 부작용으로 인해 치료를 중단하지 않았고 약물과 관련된 심각한 부작용도 없다고 부언했다.
미국에서만 약 10만명이 AAT 결핍증을 앓고 있으나 승인된 치료법은 아직 없다. 버텍스 외에도 영국에 본사를 둔 메레오 바이오파마(Mereo BioPharma)는 올해 말 AAT 약물의 중간단계 임상시험을 실시할 예정이다. 그리고 미국 바이오기업 애로헤드 파마슈티컬(Arrowhead Pharmaceuticals)도 중간단계 연구 중이다.
버텍스는 현재 폐질환자의 약 90%에게 치료 옵션을 제공하는 4가지 약물을 보유하고 있다. 지난해 매출은 62억 달러를 기록했고 올해는 약 70억 달러로 예상하고 있다.