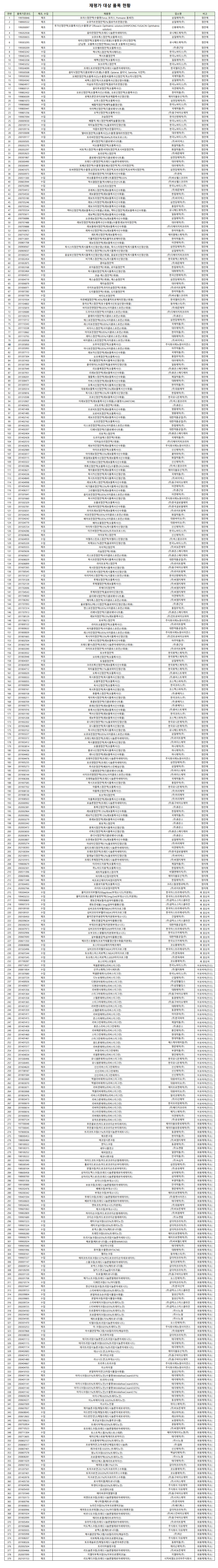
올해 의약품 동등성(생물학적 동등성, 이화학적 동등성) 재평가 대상에 제형별로 점안제 207개, 점이제 7개, 폐에 적용하는 흡입제 18개, 외용제제 147개 등으로 379개 품목이 품목허가도 취소될 수 있는 평가시험대에 올랐다.<표 참조>
생물학적ㆍ이화학적 등 시험을 통해 주성분ㆍ함량 및 제형이 동일한 두 제제에 대한 의약품 동등성을 입증해야 한다.
이번 재평가는 콜린알포세레이트 제제 257 품목 재평가 이후 1년 만에 이루어지는 대규모 의약품 평가이다.
품목 보유 업체는 재평가 신청서와 의약품 동등성 시험계획서를 오는 12월31일까지, 결과보고서는 내년 9월30일까지 식품의약품안전처에 제출해야 한다.
동등성시험에서 동등성을 입증하지 못한 품목들은 허가취소 및 회수 등의 조치를 받게 돼 향후 파장이 예상된다. 이번 재평가로 효과가 미약하거나 급여가 필요없는 약제가 대거 걸러질 전망이어서 업계가 또다시 비상이 걸렸다.
재평가 대상 점안제는 한국노바티스가 맥시덱스점안액(덱사메타손) 등 12개 품목으로 가장 많다. 이어 삼일제약 11개 품목, 국제약품ㆍ삼천당제약 8개 품목,대우제약ㆍ라이트팜텍ㆍ휴온스ㆍ휴온스메디케어, 한림제약 7개 품목, 한미약품ㆍ이연제약ㆍ제뉴원사이언스ㆍ씨엠지제약 6개 품목, 바이넥스ㆍ한국휴텍스제약ㆍ대한약품공업 5개 품목이 대상이다.
이어 종근당, 화일약품, 태준제약, 한국유니온제약, 동구바이오, 풍림무약, 디에이치피코리아, 신신제약, 아리제약이 4개 품목이다. 유니메드제약, 일동제약, 바슈헬스코리아, 대화제약, 넥스팜코리아, 한국글로벌제약, 휴비스트제약, 코스맥스파마, 한국코러스, 휴메딕스, 마더스제약이 3개 품목씩이다.
신풍제약, 한국엘러간, 제이더블유신약, 한국산텐제약, 한독, 케이엠에스제약, 동아에스티, 아주약품, 제일약품, 대웅제약, 영풍제약, 콜마파마, 대웅바이오, 비보존제약, 인트로바이오파마, 하나제약도 재평가 품목이 들어있다.
점이제는 크리스탈생명과학, 라이트팜텍 등의 7개 품목이 재평가 대상이다.
폐 흡입제는 한국아스트라제네카, 한국오츠카제약, 코오롱제약, GSK, 건일제약, 한국테바, 대한약품 등의 18개 품목이 재평가 대상이다.
외용제제는 태극제약이 아지나크림 등 10개 품목이 재평가 대상으로 가장 많다. 갈더마코리아가 7개 품목, 신신제약도 3개 품목이 들어있다.
GC녹십자, 일양약품, 에어프로젠제약, 비씨월드제약, 오스틴제약, 팜젠사이언스, 일성신약, 삼아제약, 엘지화학, 신일제약, 유유제약, 안국약품, 하원제약, 씨엠지제약, 한국신약, 동광제약, 뉴젠팜, 일리코제약, 명문제약, 나노팜, 아이큐어, 다산제약, 부광약품, 퍼슨, 한국파마, 한국프라임, 명인제약, 환인제약, 한국유니언제약, SK케미칼, 메디톡스, 위더스제약, 이연제약, 보령제약, 메디카코리아, 제엘파마, 비보존제약, 제뉴원사이언스, 에리슨제약, 동화약품, 더유제약도 재평가 품목들이 들어있다.