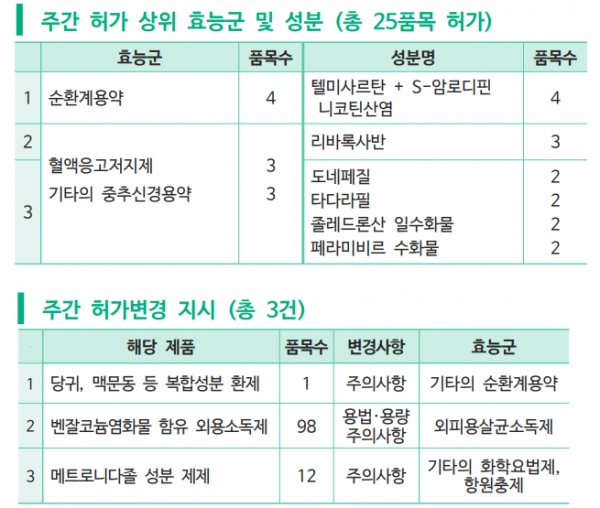
독감 치료제인 페라미비르(peramivir) 성분의 새로운 제형으로 종근당의 ‘페라원스프리믹스주’와 GC녹십자의 ‘페라미플루프리믹스주’가 자료제출의약품으로 허가되는 등 지난주(5월 31일~6월 6일)25개 품목이 식품의약품안전처 허가를 받았다.
약학정보원(원장 최종수)의 주간 허가 리뷰에 따르면 이번에 승인을 받은 종근당과 GC녹십자의 독감 치료제는 프리믹스주 제제로 기존 주사제와 달리 생리식염수 희석 과정이 필요하지 않아 희석 과정에서 발생할 수 있는 오류 및 오염 위험 감소에 기여할 것으로 기대되고 있다. 이 약은 성인 및 2세 이상 소아의 A형 또는 B형 인플루엔자 바이러스 감염증의 치료에 사용하도록 승인되었다.
식약처는 또 기존에 시판 중인 텔미사르탄+S-암로디핀 베실산염 성분의 고혈압 치료제의 염을 변경한 텔미사르탄+S-암로디핀 니코틴산염(telmisartan+S-amlodipine nicotinate) 성분의 한림제약 ‘로디엔티정’ 4개 함량(40/2.5mg, 40/5mg, 80/2.5mg, 80/5mg)이 자료제출의약품으로 허가했다. S-암로디핀(암로디핀) 또는 텔미사르탄 단독요법으로 혈압이 적절하게 조절되지 않는 본태성 고혈압에 사용하도록 승인되었다.
지난주 허가변경 지시는 3건으로 뇌졸중의 회복기 및 후유증 환자의 증상 개선에 사용되는 당귀, 맥문동 등 복합성분 환제에 대한 국외정보 검토 결과, 간기능 이상, 신장기능 이상이 있는 경우 복용 전 의사, 한의사, 치과의사, 약사, 한약사(의료전문가)와 상의해야 한다는 내용이 주의사항에 신설되었다. 더불어 약물 투여 후 어지러움, 두통, 오심, 구토, 가슴 답답함, 피부 발진, 발열 등의 이상 사례가 보고되었으며 해당 증상이 나타날 경우 복용을 중단하고 의료전문가와 상담해야 한다는 내용이 포함되었다. 이 외에도 장기간 복용하지 않아야 한다는 내용이 추가되었다.
식약처는 또 원충 및 세균 감염증 예방에 사용되는 메트로니다졸 성분 제제의 미국 FDA 안전성 정보 검토 결과, QT 간격(심실의 흥분-이완을 나타내는 기간)을 연장시킬 가능성이 있는 약물과 함께 메트로니다졸을 투여했을 때 QT 연장이 보고되었다는 내용을 ‘상호작용’ 항에 신설했다.