임상재평가 실패로 식품의약품안전처로부터 사용중단 처분은 받은 스트렙토키나제·스트렙토도르나제에 대한 정부 당국의 후속 조치가 타당한 것으로 의견이 모아졌다.
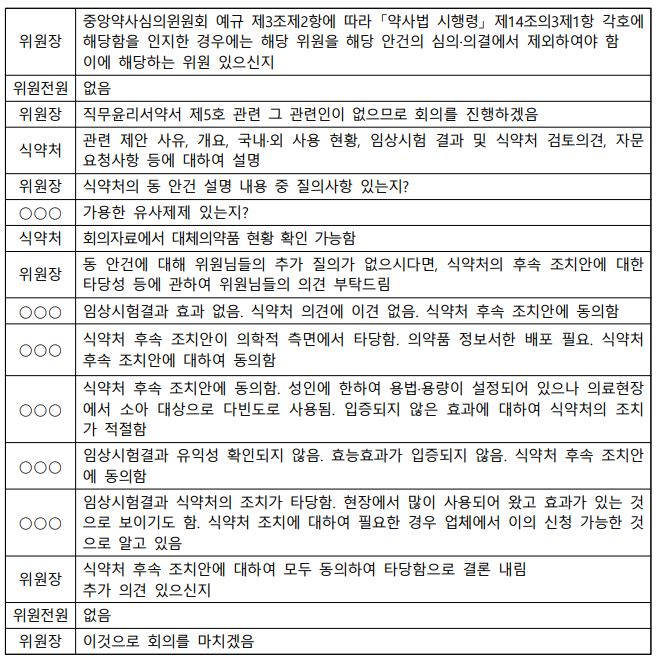
식약처가 28일 공개한 중앙약사심의위원회(중앙약심) 회의록에 따르면 임상시험 결과 효과 없음이 확인되었고 대체제도 있어 식약처 후속 조치안이 의학적 측면에서 타당하다고 참석 위원 7명이 모두 후속 조치 계획에 대해 동의해 타당성이 인정된다고 결론지었다.
식약처는 임상시험 재평가 결과 ‘호흡기 담객출 곤란’ 및 ‘발목 염증성 부종’에 대해 효과를 입증하지 못한 ‘스트렙토키나제·스트렙토도르나제’ 제제의 사용중단과 다른 치료 의약품 사용을 권고하는 의약품 정보 서한을 지난달 31일 배포했었다.
이날 회의에서 한 위원은 “ 성인에 한하여 용법·용량이 설정되어 있으나 의료현장에서 소아 대상으로 자주 사용된다”면서 “입증되지 않은 효과에 대하여 식약처의 조치가 적절하다”고 말했다.
또 다른 위원도 “현장에서 많이 사용되어왔고 효과가 있는 것으로 보이기도 하지만 식약처 조치에 대하여 필요한 경우 업체에서 이의신청 가능한 것으로 알고 있다”면서 “식약처 조치가 타당하다”고 밝혔다.
한편 스트렙토 제제는 지난해 급여재평가 결과 임상적 유용성이 불충분하다는 판정을 받았지만 임상재평가가 진행 중인 점을 고려해, 유효성을 입증하지 못할 경우 급여 일부를 공단에 환수하는 조건에 합의한 품목을 대상으로 1년간 조건부로 평가를 유예하기로 했었다.
결국에 2개의 적응증 모두 유효성 입증에 실패하면서 환수 협상을 통해 급여 일부를 환수 당하게 됐다. 스트렙토제제를 보유한 제약사 37곳 중 22곳은 건강보험공단과 22.5%의 환수율과 환수 기간 1년에 합의했었다.
업계에선 스트렙토제제가 지난해 272억원의 외래 처방실적을 바탕으로 환수금은 61억원 규모로 알려졌다.