의약품 허가ㆍ특허연계제도가 지난 3월부터 시행된 후 우선판매허가 첫 품목은 아모잘탄 제네릭으로 나타났다.
식품의약품안전처(처장 김승희)는 한ㆍ미 자유무역협정(FTA)에 따른 의약품 허가ㆍ특허연계제 실시 이후 처음으로 휴온스와 JW중외신약 등 13개 제약사 34품목에 대해 우선판매품목으로 허가한다고 8일 밝혔다. <표 참조>
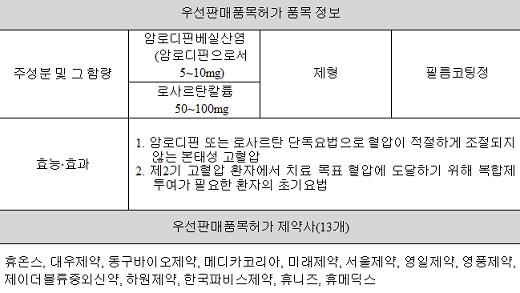
이번에 우선판매허가되는 품목은 암로디핀베실산염과 로살탄칼륨의 복합제인 '아모잘탄정'(한미약품)으로, 조성물 특허를 침해하지 않았다는 특허심판원의 확인을 거쳤다.
이들 품목은 용량별 3가지 종류로 34품목이며 제형은 모두 필름코팅정이다.
34품목은 암로디핀 5mgㆍ로살탄 50mg(13품목), 암로디핀 5mgㆍ로살탄 100mg(12품목), 암로디핀 10mgㆍ로살탄 50mg(9품목)이다.
앞으로 9개월 후인 내년 2월8일까지 이 복합제는 이번에 우선판매품목으로 허가된 품목만을 판매할 수 있게 된다.
34품목과 같은 날 허가 신청된 동일 품목도 우선판매품목허가를 받으면 판매 가능하다.
이번 우선판매허가 품목의 공동 개발에 참가한 13개 제약사 중 12개사는 매출이 1000억원 미만(2013년 기준)인 중소제약사들로 한ㆍ미 FTA 시행 뒤인 2012년부터 공동으로 개발에 들어가 지난해 의약품 허가특허 심판 등을 진행했다.
식약처는 "이번 우선판매허가된 품목은 중소제약사들이 허가ㆍ특허연계제 시행 초기부터 공동으로 전략적인 제품 개발과 특허 도전에 성공한 사례"라며 "앞으로도 국내제약사가 우선판매품목허가를 활발히 준비할 수 있도록 맞춤형 교육과 특허정보를 지속적으로 제공하겠다"고 말했다.
이어 "이번 허가는 보험약가 인하 효과도 있어 국민들의 의료비 지출 감소에도 도움이 될 것"이라고 기대했다.
우선판매품목허가는 특허 의약품에 대응해 개발한 후발약품의 품목허가를 최초로 신청하고, 특허 쟁송에서 이긴 제약사가 특허권의 존속기간 내에서 9개월간 해당 의약품을 우선 판매할 수 있는 제도로 일종의 국내 제약산업 보호장치다.

