삼성바이오에피스(대표 고한승)가 희귀질환 치료제 'SB12'(솔리리스 바이오시밀러, 성분명 에쿨리주맙) 의 임상 3상에 본격 착수했다.
회사 측은 SB12의 임상 3상시험 계획을 구체화하고 이를 글로벌 임상시험 정보 사이트를 통해 공개했다.
삼성바이오에피스는 독일에서 진행된 SB12의 임상 1상을 올해 초 완료한 바 있다. 임상 3상은 오리지널 의약품과의 유효성, 안전성, 약동학과 면역원성을 비교하는 것이며 한국을 포함한 총 10개국의 환자 50명을 대상으로 2021년 7월까지 진행될 예정이다.
한편 '솔리리스'(Soliris)는 미국의 희귀난치성 질환 치료제 전문 제약사 알렉시온(Alexion)이 개발한 '발작성 야간 혈색소뇨증(PNH)'치료제다. PNH 진환은 혈관 내 적혈구가 파괴되면서 혈전이 생기고 야간에 용혈 현상이 생겨 혈색 소변을 보이는 증상을 동반하는 희귀질환이다.
솔리리스는 대표적인 고가 바이오의약품으로 알려져 있으며 지난 해 글로벌 매출 규모는 35억6300만 달러(약 4조3000억원)에 달한다.
업계에 따르면 국내 솔리리스 1 Vial(30㎖) 의 가격은 비급여 기준 약 600만원으로 성인 기준 투약 비용이 연간 약 5억원 규모에 달하는 것으로 알려져 있다.
이 약의 특허는 유럽에서는 2020년 6월, 미국에서는 2021년 3월에 만료 될 예정이다.
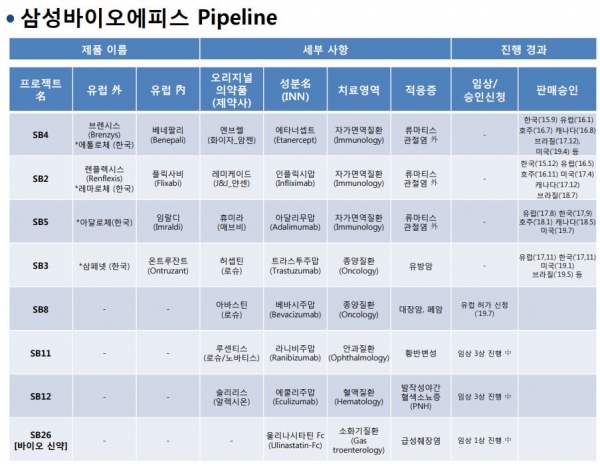
삼성바이오에피스는 SB12외에도 황반변성ㆍ류마티스 관절염ㆍ유방암 등 다양한 파이프라인을 가지고 있다.<표 참조>
삼성바이오에피스 관계자는 "자가면역질환과 종양질환 치료제를 개발하며 쌓은 역량을 바탕으로 희귀질환 치료제로 개발 분야를 넓혔다”며 “SB12의 성공적 개발을 통해 고가의 바이오의약품에 대한 환자들의 치료 접근성을 확대할 수 있도록 하겠다” 고 밝혔다.