식품의약품안전처(처장 이의경) 식품의약품안전평가원은 8월 21일~23일까지 오송첨단의료산업진흥재단 C&V센터(충북 청주시 소재)에서 ‘과학적 근거 기반 의약품 개발 및 허가’를 주제로 ‘2019년 식품의약품안전평가원-미국약물정보학회 워크숍’을 개최한다고 19일 밝혔다.
미국약물정보학회(DIA)는 1964년 창립하여 80개국에 회원을 보유하고 있으며 의약품 개발ㆍ허가 관련 컨퍼런스, 정기 훈련과정(120여개), 저널 등을 운영하고 있다.
이번 워크숍은 미국의 규제ㆍ개발동향과 국내 의약품의 해외시장 진출 성공사례 공유를 통해 우리나라 제약ㆍ바이오업계의 글로벌 경쟁력을 높이기 위해 마련했다.
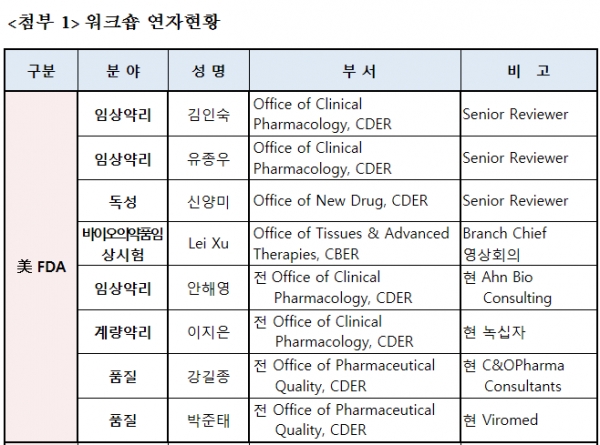
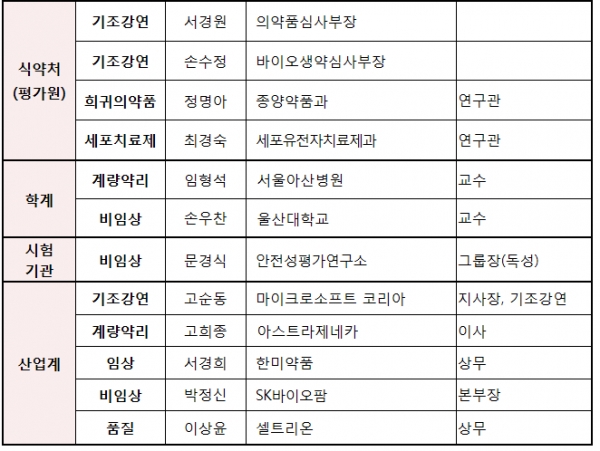
특히 최근 개발이 활발한 희귀ㆍ난치성 질환 치료제와 바이오의약품을 중심으로 미국 FDA 전ㆍ현직 허가심사자를 비롯해 국내 석학과 제약 전문가가 참여하여 의견을 나눌 계획이다. 이 워크숍은 20명의 연자(美 FDA 연자 8명)를 초청하여 7개 세션으로 진행할 예정이다.
워크숍의 주요 내용은 ▲희귀질환 의약품의 비임상ㆍ임상시험과 계량약리학 ▲세포·유전자치료제 등의 품질ㆍ비임상·임상시험이며 패널토의에서는 품질ㆍ비임상ㆍ임상시험 분야별로 양국 규제기관의 심사 시 고려사항에 대해 깊이 있는 논의를 진행할 예정이다.
한편 지난해에는 ‘의약품 개발과 허가에서 기회와 도전’ 주제로 연자 16명(FDA 4명)에 4개 세션으로 진행됐다.<표 참조>
이번 행사는 ‘워크숍’과 함께 비공개 ‘한ㆍ미 허가심사자 패널토의’(8.23)로 나누어 진행한다.
주요 강연은 첫날 ▲인공지능 활용 의약품개발 <고순동 마이크로소프트 한국 지사장> ▲항암제ㆍ소아용약 비임상시험 미국 심사사례 <신양미 FDA 신약심사부서 선임심사관 등> ▲희귀질환 의약품의 임상시험 심사방향 <김인숙 FDA 임상약리부서 선임심사관 등> ▲신약개발에 필수적인 계량약리 모델링 <이지은 전 FDA 임상약리부서 선임심사관 등>
2일차에는 ▲세포ㆍ유전자치료제 허가규정과 임상시험 심사방향 <레이수 FDA 첨단바이오의약품부서 과장 등> ▲바이오의약품의 개발 시 제조ㆍ품질자료 <이상윤 셀트리온 상무 등> ▲희귀의약품 해외기술수출 성공전략 <서경희 한미약품 상무 등>내용으로 강연을 한다.
식약처는 "이번 워크숍이 국내 의약품 연구개발과 허가심사 체계의 규제조화에 도움이 될 것으로 기대하며 앞으로도 안전이 확보된 우수한 의약품 개발을 위한 워크숍 등 다양한 지원 프로그램을 운영하겠다"고 밝혔다.