미국에서 허가된 신약이 10년간(2010~2019년) 2배나 급증한 것으로 나타났다.
한국바이오경제연구센터와 미국 FDA 의약품평가센터에 따르면 미국에서 작년 신약 허가 건수가 48건으로 2010년(21건)보다 128.5% 증가했으며, 신약 중 바이오의약품이 10건ㆍ희귀약이 21건으로 각각 20%와 40% 이상 차지했다.
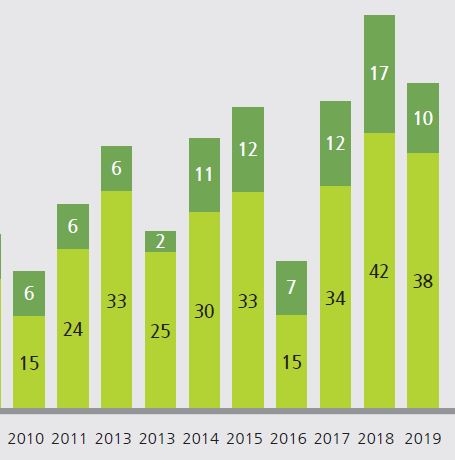
미국에서 작년 허가된 신약 중 화학합성의약품은 38건이었고, 2010년엔 화학의약품이 15건, 바이오약품이 6건으로 각각 집계됐다. <그래프 참조>
제약사별론 지난해 노바티스가 5건으로 가장 많은 데 이어 애브비와 로슈 각 3건, 화이자 2건 등의 순이었다.
지난해 허가된 주요 글로벌 제약사(美ㆍ유럽)의 신약은 상반기엔 사노피의 혈액응고질환 치료제 '카블리비', 노바티스의 뇌전증 치료제 '에가탄'과 다발성경화증 치료제 '메이젠트', 암젠의 골다공증 치료제 '이베니티', 얀센의 방광암 치료제 '발버사', 애브비의 건선 치료제 '스카이리치', 화이자의 다발신경병증 치료제 '빈다켈', 노바티스의 유방암 치료제 '피크레이', 로슈의 거대 B-세포 림프종 치료제 '폴리비' 등이다.
하반기엔 MSD의 항균 복합제 '리카브리오', 바이엘의 전립선암 치료제 '누베카', 화이자의 다제내성 결핵 치료제 '프레토마니드', 로슈 항암제 '로즐리트렉', 애브비 류마티스관절염 치료제 '린보크', 로슈ㆍBMS의 골수섬유증 치료제 '인레빅', 갈더마의 여드름 치료제 '아클리프', 노바티스의 황반변성 치료제 '베오부'와 겸상적혈구질환 치료제 '아닥베오', 릴리 편두통 치료제 '레이보우', 세엘진ㆍBMS의 빈혈 치료제 '레블로질', 애브비(엘러간)의 편두통 치료제 '우브렐비'가 신약으로 허가를 받았다.
일본 제약사론 쿄와기린의 파킨슨병 치료제 '누리안즈', 시오노기 항균제 '페트로자', 아스텔라스의 요로상피세포암 '패드세브', 에자이의 불면증 치료제 '데이비고', 다이이찌산쿄ㆍ아스트라제네카의 유방암 치료제 '엔허투'가 포함됐다. 중국 바이오제약사인 베이진이 개발한 외투세포림프종 치료제 '브루킨사'도 미국에서 지난해 허가됐다.
국내 기업으론 SK바이오팜의 수면장애 치료제 '수노시'와 뇌전증 치료제 '엑스코프리'가 지난해 잇따라 미국에서 허가를 받아 세계 의약계로부터 관심을 끈 바 있다.
센터 관계자는 "미국의 지난해 신약 허가 건수가 최대 허가 건수를 기록한 2018년(59건) 대비 줄었지만, 9~10년 전보다 크게 늘었다"며 "특히 바이오신약과 희귀의약품의 허가가 증가세를 보이고 있다"고 말했다.

