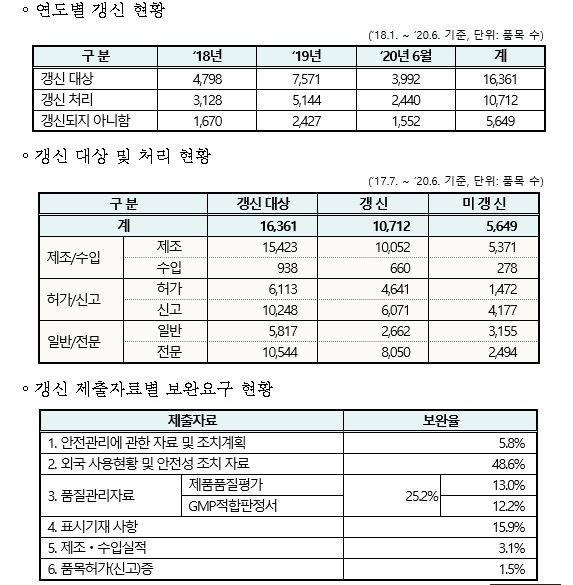
식품의약품안전처는 의약품 품목 갱신 제도가 본격 시행된 2018년 이후 올 6월까지 약 3년간 5649개 품목을 정비했다고 25일 발표했다. <표 참조>
의약품 허가ㆍ신고 유효 기간을 5년으로 정한 이 제도는 약품의 주기적ㆍ체계적인 안전관리를 위해 2013년 도입된 뒤 2018년부터 본격적으로 실시되고 있다.
이와 관련해 식약처는 이 기간 동안 갱신 대상 품목 1만6361개 중 35%를 정비해 1만712개(전체의 65%) 품목이 갱신된 것으로 집계했다고 밝혔다.
갱신 대상 의약품은 총 4만6063개(작년 12월 기준) 품목이며, 산술적으로 해마다 약 7000품목을 갱신 대상으로 하고 있다.
식약처에 따르면 허가 갱신을 통해 품목이 정비된 주요 사유는 생산ㆍ수입 실적이 없는 품목이 64%(3612개)로 많았다.
또 ▲수입보다 제조 품목이 대부분을 차지(95%ㆍ5371개)했고 ▲허가 품목(26%ㆍ1472개)보다는 신고 품목(74%ㆍ4177개)이 ▲전문의약품보다는 일반의약품 비율이 높았다고 식약처는 설명했다.
이 기간 운영해온 의약품 품목 갱신의 주요 성과론 허가만 받고 생산ㆍ수입하지 않은 상당수 품목을 정비함으로써 소비자에게 실제 공급ㆍ사용되는 의약품을 중심으로 효율적인 안전관리를 할 수 있는 기반을 마련하였다는 데 의의가 있다고 식약처는 평가했다.
식약처는 민관협의체 등 업계와 지속적으로 소통, 갱신을 위한 자료 보완을 요구한 품목의 비율이 올해 30%까지 낮아졌다고 강조했다.
이에 식약처는 이 제도가 의약품의 시판 후 안전 및 품질 관리 현황을 주기적으로 확인할 수 있는 제도로 자리매김할 수 있도록 지속적으로 개선을 추진 중이다.
내년 3월부터는 안전관리에 관한 자료로 제약사 내 시판 후 안전관리를 담당하는 안전관리책임자의 분석ㆍ평가 결과 제출을 의무화하고, 관련 안전성 정보 보고자료 일체도 함께 제출토록 제도가 개선된다.