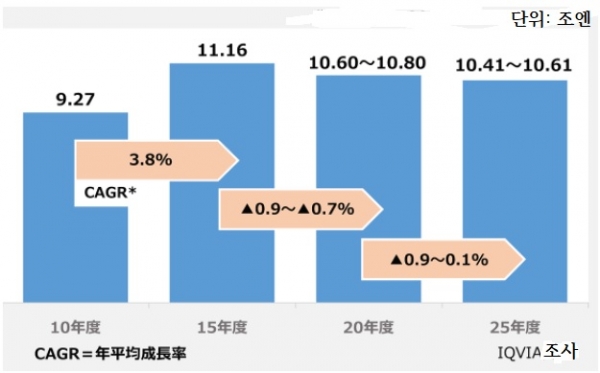
일본 의약품 시장이 2021년에는 완만한 마이너스 성장을 보일 것으로 예측됐다.
일본 아이큐비아(IQVIA)는 매년 약가 개정과 연관된 의료비 절감액이 2020~2025년에 3조엔 이상에 이르고 코로나19에 따른 진료 패턴 변화도 당분간 지속돼 의약품 시장이 완만한 마이너스 성장이 예상된다고 밝혔다.
일본 제약단체연합회 등 일본, 미국, 유럽 제약단체들은 새해 일본 약가 개정에 대해 “약가 제도 예측 가능성을 현저하게 훼손한 것으로 도저히 납득할 수 없다”며 “장기 등재 품목에 끼치는 영향도 크고 빅 파마를 중심으로 매각 움직임은 계속될 것”이라고 지적했다. 이들은 또 “장기등재 품목의 수익에 의존하는 중견 제약기업엔 생존이 걸린 대목”이라고 밝혔다.
디지털 헬스와 질병 전단계인 ‘미병(未病) 비즈니스’ 등 신규 사업의 창출을 향한 움직임도 활발해질 것으로 전망됐다. 지난해엔 피트니스 서비스에 참가한 아스텔라스와 간호ㆍ치매 부문을 중심으로 외부와 잇따라 제휴를 맺은 토와약품(東和薬品) 등의 움직임이 눈에 띄었다.
아스카제약과 사와이제약(沢井製薬)은 신규 사업의 육성을 위해 올해부터 지주 회사 체제로 전환할 예정이다.
한편 일본에서 20만명 이상이 감염돼 3000명 이상 사망자를 낸 코로나19 백신 접종은 2월부터 실시할 예정이다. 화이자와 바이오엔텍이 공동 개발한 mRNA 백신은 2월 하순 접종 개시를 목표로 하고 ▲의료 종사자(400만명) ▲65세 이상 노인(3600 만명) ▲기저 질환자(820만명), ▲노인 시설 근무자(200만명), ▲60~64세(750만명) 순으로 접종한다.
일본 정부는 화이자로부터 올해 6월까지 1억2000만회 분(6000만명 분)을 공급 받기로 합의했고 모더나로부터는 9월까지 5000만회 분(2500만명 분), 영국 아스트라제네카에서 올해 초에 1억2000만회 분(6000만명 분)을 공급받는다.
한편 일본에선 새해엔 편두통 적응증에 3개의 항체 의약품 등 신약이 속속 출시될 전망이다.
항암제는 2019년 5월 승인된 '킴리아(Kymriah)'에 이어 2,3번째 CAR-T 세포 요법제가 승인될 전망이다. 다이이찌산쿄의 ‘예스카타(Yescarta)'와 BMS의 ‘리소-셀(liso-cel)' 중 예스카타는 지난해 12월 후생노동성 부회에서 승인을 받았다. 또 인사이트 재팬(Incyte Japan)은 FGFR 억제제 담관암치료약 ‘페미가티닙(Pemigatinib)'과 에자이의 EZH2 유전자 변이 양성 여포성 림프종 치료제 ‘타즈베릭(Tazemetostat)'도 승인을 앞두고 있다.
중추 신경계 영역에서 CGRP를 대상으로 한 편두통 치료제 ▲일본 일라이 릴리의 ’엠겔러티‘(Emgality 갈카네주맙) ▲오츠카 제약의 ’아조비‘(Ajovy 프레마네주맙) ▲암젠의 ’에이모빅‘(Aimovig 에레누맙) 등 3개의 항체 의약품이 승인을 앞두고 있다. 또 주가이제약의 첫 경구용 척수성 근위축증(SMA) 치료제 ’리스디플람‘(Risdiplam)도 주목된다.
이와함께 에자이와 바이오젠은 알츠하이머병을 치료제 항 아밀로이드β 항체 ’아두카누맙(Aducanumab)’을 신청했다. 다만 미국 FDA 자문위원회가 승인에 부정적인 견해를 나타내고 있어 일본 후생노동성의 판단이 주목된다.
올해는 그밖에도 새로운 작용 기전의 당뇨병 치료제 ‘이메글리민’(Imeglimin 다이니폰스미토모)과 급성간성포르피린증(AHP)의 첫 정밀 RNAi 치료제 '기브라리'(Givlaari 앨나일람 저팬), 부갑상선호르몬(PTH) 제제 골다공증 신약 ‘아발로파라티드’(Abaloparatide 테이진파마)도 승인될 전망이다.