지난해 6월 미국 FDA에서 ‘에듀헬름’(Aduhelm)이 조건부 승인 되면서 유효성과 약값 논란을 빚은 알츠하이머 치료제를 뒤이을 새로운 약물개발이 주목을 끌고 있다. 현재 전 세계에서 126개 후보물질을 대상으로 152건의 임상시험이 진행되고 있다. 이중 3상은 41건의 임상이 실시되고 있는 것으로 알려졌다.
한국연구재단은 최근 ‘알츠하이머 치매 치료_기초연구본부 선정 R&D 이슈’ 연구 동향 브리프에서 국내외 기초 연구와 치료제 개발을 소개했다.

◇17년간 알츠하이머 치료제 개발 소식 없어
현재 알츠하이머 치매 치료제는 없으나 3종의 아세틸콜린분해효소 억제제, 1종의 NMDA 수용체 길항제 약물만이 미국 FDA 승인하에 증상개선 목적으로 사용 중이다. 1993년에 아세틸콜린분해효소 억제제가, 10년 뒤인 2003년에는 NMDA 수용체 길항제가 FDA의 승인을 받아 임상 현장에서 사용되었지만 이후 17년이 넘도록 이렇다 할 알츠하이머 치매 신약 개발의 소식이 없다.
▲아세틸콜린분해효소 억제제(ACEI)=정상인의 경우, 뇌의 신경세포에서 아세틸콜린이라는 신경전달물질이 적절히 분비되어 기억력이 유지되고 학습이 가능하지만 알츠하이머병 환자의 뇌에서는 아세틸콜린 합성과 대사가 감소되어 기억력과 같은 인지기능이 떨어지게 된다. 아세틸콜린분해효소 억제제 계통의 약물들은 시냅스에서 가용한 아세틸콜린의 양을 증가시키는 기전으로 치매 환자의 인지기능을 일부 호전시킬 수 있는 것으로 알려졌다.
도네페질(Donepezil), 리바스티그민(Rivastigmine), 갈란타민(Galantamine) 등 병의 진행을 막을 수는 없고 그 경과를 약 6개월~2년 이상 늦출 수 있다고 하지만 명확한 근거는 없는 실정이다.
▲NMDA 수용체 길항제(NMDA receptor antagonist)=글루타메이트(glutamate)라는 신경전달물질이 과도하게 활성화되면 NMDA 타입의 글루타메이트 수용체를 통하여 신경세포 손상 및 사멸이 일어날 수 있다. 따라서 NMDA 수용체를 억제함으로써 신경세포 사멸을 억제하고 병의 진행을 막을 수 있을 것으로 알려졌다.
메만틴(Memantine)이 경증보다는 중등도 및 중증 알츠하이머병 환자에게서 신경세포 손상을 막고 남아있는 신경세포의 생리적 기능을 복원시켜 증상 호전을 기대한다.
▲기타 보조약물(항산화제)=노화와 세포 사멸의 과정에는 산화 현상이 일어나고 이 과정에서 발생하는 독성 산소 라디칼이 알츠하이머병의 발병 기전에 관여할 수 있다. 단가아민 산화효소 억제제인 셀레길린(Selegiline)이나 비타민 E(고용량)가 사용될 수 있으나 효능에 있어서 상당한 논란이 있다.
◇최근 개발되고 있는 치매 치료제는?
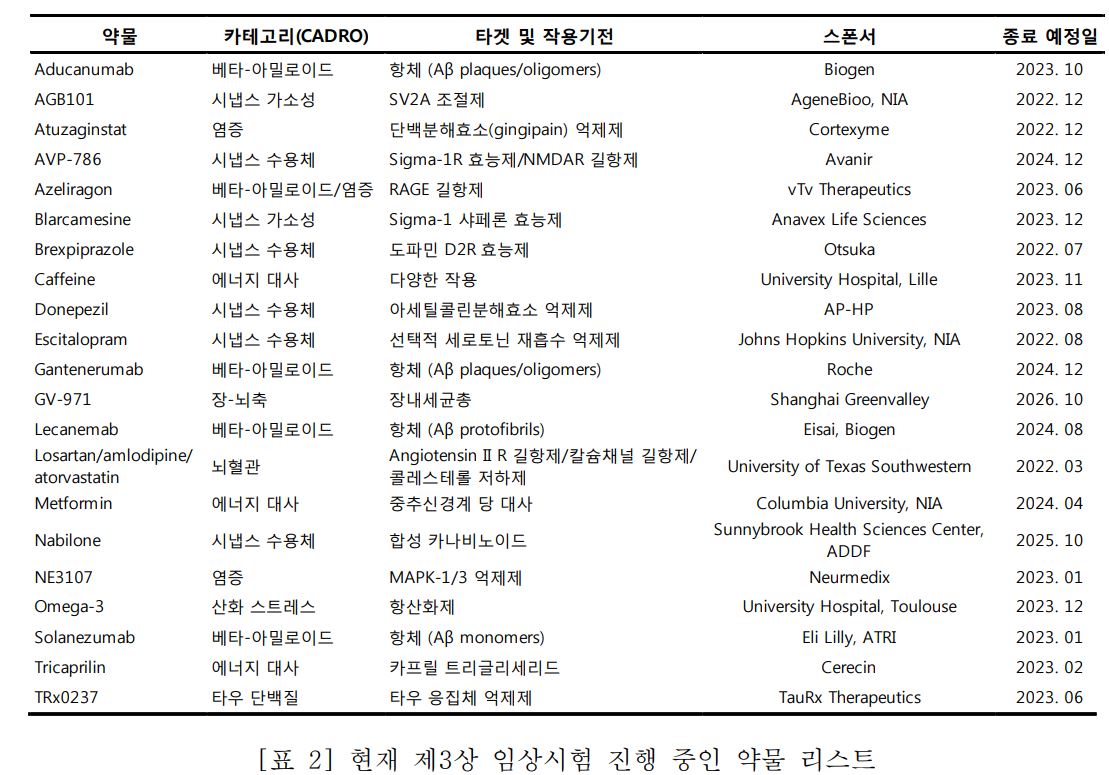
현재(2021년 1월 5일 기준) 전 세계에서 126개 후보물질을 대상으로 152건의 임상시험이 진행되고 있다. 3상에 진입한 물질 28개를 대상으로 41건의 임상이 실시되고 있으며 2상은 74개의 후보물질로 87건의 임상시험, 1상 단계에서는 24개의 후보물질로 24건의 임상이 진행 중이다. 임상을 위해서는 3만8000명 이상의 피험자가 필요하다.
이 중 알츠하이머 치매 진행을 늦추거나 질병을 개선하는 근원적 치료제(DMTs)가 104개로 전체 후보물질의 82.5%를 차지하고 있으며 16개(15.4%)는 베타-아밀로이드 표적, 11개(10.6%)는 타우 단백질을 표적으로 하고 있다. 증상개선 약제(symptomatic treatments) 중 13개 약제(10.3%)는 인지기능 개선을 목표로하고 13개 약제(7.1%)는 신경정신 행동증상 개선을 목표로 하고 있다.
최근 임상 추세는 다양한 생물학적 단계를 표적으로 하는 질환 조절 연구, 바이오마커 활용 연구, 용도변경 약물(repurposed agents)을 이용한 연구가 늘었다는 특징이 있다.
미국에서는 30대~50대에 증상이 나타나는 우세유전 알츠하이머병(DIAD) 증상 발생 전 및 발생 후 DIAD 환자를 대상으로 베타-아밀로이드 제거 항체인 '솔라네주맙'(solanezumab)과 '간테네루맙'(gantenerumab) 임상 3상에서 간테네루맙은 증상 발생 전ㆍ후 대상 모두에게서 아밀로이드 플라크 및 타우를 감소시켰으나 인지기능 개선 등 치료 효과는 없는 것으로 나타났다. 다만 고용량 항체 투여가 안전하다는 점, 무증상 그룹에서 발생 가능한 인지기능 저하가 없었다는 점은 긍정적 요소다.
간테네루맙은 2차 평가에서 치매 바이오마커 감소 효과 확인되면서 로슈(Roche)는 미국 FDA와 신속승인 협의 중이며 추가 효과 입증되면 에듀헬름을 이을 유망한 치매 치료제로 재부상할 수 있다.
바이오젠에서 개발한 타우 항체 ‘고수라네맙’(gosuranemab, BIIB092)은 2상에서 실패했으며 BMS는 프로테나(Prothena)로부터 타우 미세소관 결합 부위를 타깃으로 한 타우 항체 ‘PRX005’를 인수, 지난해 6월 24일 임상 에 들어갔다. 또 일라이 릴리(Eli Lilly)는 아밀로이드 플라크 항체 ‘도나네맙(donanemab)’에 대한 임상 2상 1차 평가에서 인지기능 저하 32% 개선했다. 릴리는 임상 규모를 늘려 3상 추진 중이며 2023년 상반기에 결과 나올 예정이다.
미국에서는 미세아교세포(microglia)가 차세대 알츠하이머 치매 치료 타깃으로 새롭게 부각하고 있다.
미세아교세포는 자가 포식작용을 통해 죽어가는 대뇌 불순물, 신경세포나 시냅스 등을 제거하는 역할을 담당하는 대뇌에 존재하는 면역세포다. TREM2는 미세아교세포의 표면에 특이적으로 발현되는 수용체로 2013년 대규모 인간 유전체 연구 결과, 후기 알츠하이머 치매 위험인자로 밝혀지면서 최근 가장 주목받고 있는 차세대 알츠하이머병 치료 타깃이다.
애브비(AbbVie)와 알렉토(Alector)社는 TREM2 표적 항체 'AL002' 임상 2상을 지난해 11월 시작했으며 결과는 2023 여름에 나올 예정이다. 비질 뉴로사이언스(Vigil Neuroscience)는 암젠(Amgen)으로부터 TREM2 활성화 항체와 저분자화합물을 사들여 임상 시험 중이다. 또 뉴랄리(Neuraly 디앤디파마텍)社는 GLP-1 수용체 표적 약물 NLY01은 파킨슨병 대상 임상 2상을 진행 중이며 알츠하이머성 치매 대상으로 FDA 임상 2b를 승인받아 진행할 예정이다.
국내에서는 새로운 베타 아밀로이드-타우 독성 신호 매개체 발굴을 모색하고 있다. 서울대학교 연구팀은 알츠하이머 치매의 가장 핵심적인 두 가지 원인인 베타-아밀로이드 축적과 타우 병리간의 상호관계(Abeta-Tau axis)의 연결고리에 해당하는 새로운 Plexin-A4 단백질을 발굴하고 이에 의한 치매 발병 기전을 제시했다.
베타 아밀로이드가 타우 단백질을 과인산화시켜 응집을 촉진하고 독성을 띠도록 변성 시키는데 Plexin-A4 단백질이 해당 독성 신호를 전달하는 주요 매개체임을 확인했다.
Plexin-A4 유전자를 결손 시켰을 때 베타-아밀로이드에 의해 유도되는 인산화 효소인 CDK5-p35를 통한 타우의 과인산화와 변성 및 인지기능 저하가 억제됐다. 따라서 Plexin-A4 및 관련 신호전달 경로를 조절하여 알츠하이머 치매의 진행을 억제할 수 있음을 보여줬다.