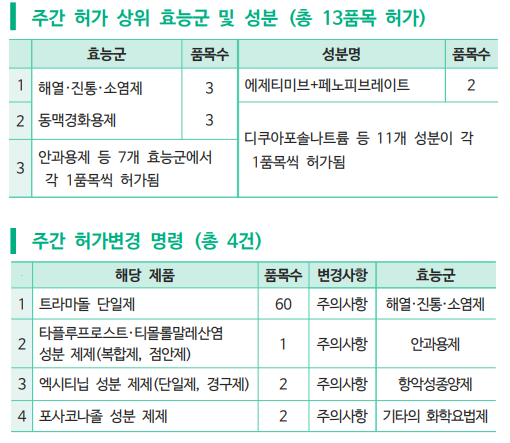
이번 주(6월 20일~26일)에 해열ㆍ진통ㆍ소염제 3개 품목 등 13개 품목이 식품의약품안전처 승인을 받았다.
약학정보원(원장 김현태)이 28일 발표한 주간 허가 리뷰 중에서 엘지화학의 당뇨병 치료 신규 복합제 ‘제미다파정’이 가장 눈에 띈다. 이 약은 SGLT-2 억제제 계열의 다파글리플로진(dapagliflozin)과 DPP-4 억제제 계열의 제미글립틴타르타르산염(gemigliptin tartrate sesquihy-drate) 성분을 함유한 신규 복합제로 자료제출의약품으로 허가되었다.
제미다파정은 국내에서 유일한 성분 조합으로 2012년 국산 신약 19호로 허가된 ‘제미글로정’50mg(제미글립틴타르타르산염1.5수화물)에 다파글리플로진을 추가한 복합제다. 이 약은 제미글립틴과 다파글리플로진의 병용투여가 적합한 제2형 당뇨병 환자의 혈당 조절을 향상시키기 위해 식사요법 및 운동요법 보조제로 사용하도록 승인되었다.
제미다파정은 식사와 관계없이 1일 1회 1정을 투여한다. 단 제미글립틴이나 다파글리플로진 또는 첨가제에 대한 과민반응 병력이 있는 환자, 제1형 당뇨병 또는 당뇨병성 케톤산증 환자, 투석
환자 등에게 사용해서는 안된다.
한편 식약처는 마약성 진통제인 '트라마돌' 단일제의 안전성 정보 검토 결과 기존 문구인 ‘트라마돌은 의존성이 낮다’라는 내용이 ‘경고’ 항에서 삭제되었다.
또 녹내장 및 고안압 환자의 안압 감소에 사용되는 타플루프로스트+티몰롤말레산염 성분 제제(복합제, 점안제)의 재심사를 위한 시판 후 조사(6년간, 619명 대상) 결과, 이상사례 발현율은 20.52%로 이 중 인과관계를 배제할 수 없는 예상하지 못한 약물 이상반응으로 결막 자극, 눈밑 다크서클, 각막 색소 침착, 피부 변색, 소양증 등이 보고되었다.